
【题目】在一密闭容器中,反应aA(g) ![]() bB(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了
B.物质A的转化率增大了
C.物质B的质量分数增加了
D.a >b
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一 沉淀分离.其流程图如下(1)沉淀的化学式:沉淀1__________沉淀2__________沉淀3__________;写出混合液与A反应的离子方程式 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用480mL 0.1mol/L的硫酸铜溶液,配制时应选择的容量瓶的规格和需要称量的溶质的质量分别为
A.480mL容量瓶,7.68g硫酸铜 B.480mL容量瓶,12.0g胆矾
C.500mL容量瓶,12.5g硫酸铜 D.500mL容量瓶,12.5g胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A.加热完毕后,用嘴吹灭酒精灯
B.过滤时,漏斗下端紧贴烧杯内壁
C.给烧杯加热时,不需要垫上石棉网
D.用托盘天平称量 NaOH 固体时,被称量的 NaOH 固体放在滤纸上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O4![]() 2NO2△H>0)
2NO2△H>0)
(a)将两容器置于沸水中加热;
(b)在活塞上都加2kg的砝码。
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
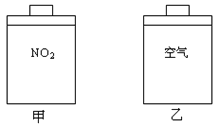
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,4个容器中分别装有4种气体,已知各容器中的气体和容器的容积分别是a.CO2 100 mL;b.O2200 mL;c.N2 400 mL;d.CH4 600 mL,则4个容器中气体的质量由大到小的顺序是
A. a>b>c>d B. b>a>d>c C. c>d>b>a D. d>c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体不可缺乏的元素,为了防止碘缺乏,市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4![]() 3I2+3H2O+3K2SO4。
3I2+3H2O+3K2SO4。
请回答下列问题:
(1)该反应中氧化剂是__________,每生成1 mol I2转移电子物质的量是__________。
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的苯,振荡,观察到的现象是______________________________。
(3)在容量瓶的使用方法中,下列操作正确的是____________(填字母)。
A.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线
1~2 cm处,用胶头滴管加蒸馏水至刻度线
B.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
C.使用容量瓶前检验是否漏水
D.容量瓶用水洗净后,再用待配溶液洗涤
(4)用容量瓶配制一定物质的量浓度的稀硫酸,下面操作造成所配稀硫酸溶液浓度偏高的是______(填字母)。
A.转移时没有洗涤烧杯、玻璃棒
B.溶解的时候溶液没有冷却到室温就转移并定容
C.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
D.向容量瓶加水定容时眼睛俯视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;B、C、D同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:(相关问题用元素符号表示)
(1)写出E的基态原子的电子排布式________________________。
(2)B与C可形成化合物BC和BC2,BC2属于__________(填“极性”、“非极性”)分子,1 mol BC含有π键为____________________mol。
(3)由元素A、C、G组成的离子[G(A2C)4]2+在水溶液中显天蓝色,不考虑空间结构,[G(A2C)4]2+的结构可用示意图表示为__________(配位键用→标出)。
(4)测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的原因是_______。
(5)由元素A、B、F组成的原子个数比9 : 3 : 1的一种物质,分子中含三个相同的原子团,其结构简式为________________,分子中F原子的杂化方式为__________,该物质遇水爆炸,生成白色沉淀和无色气体,反应的化学方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com