
���� ��1���ȳ�ȥ���е�Ca2+��Mg2+��SO42-�����ʣ������Ȼ�����ȥ��������ӣ��ټ�̼���Ƴ�ȥ���������Ӽ������ӣ�NaOH��ȥþ���ӣ�
��2��NaClO3�����ᷴӦ����ClO2��Cl2��ClԪ�صĻ��ϼ���+5�۽���Ϊ+4�ۣ�ClԪ�صĻ��ϼ���-1������Ϊ0����ϵ����غ���㣮
��� �⣺��1��������ʳ��ˮ�Ʊ������ƣ����ڵ���ʳ��ˮ���ȳ�ȥ���е�Ca2+��Mg2+��SO42-�����ʣ��ڳ��Ӳ���ʱ��������ˮ���ȼ��������BaCl2����ȥ��������ӣ����������ٲ������ټ��������Na2CO3��NaOH����ַ�Ӧ����һ����ȥ���ʴ�Ϊ��BaCl2��Na2CO3��
��2��NaClO3�����ᷴӦ����ClO2��Cl2��ClԪ�صĻ��ϼ���+5�۽���Ϊ+4�ۣ�ClԪ�صĻ��ϼ���-1������Ϊ0��������ClO2��Cl2�����ʵ����ֱ�Ϊx��y��
�ɵ����غ��֪��x����5-4��=y��2��[0-��-1��]�����x��y=2��1���ʴ�Ϊ��2��1��
���� ���������ʵ��Ʊ�������������ᴿ���������з�Ӧ�ļ��㣬Ϊ��Ƶ���㣬��������֮��ķ�Ӧ��������ԭ��Ӧ�е����غ�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� �Լ� | T1/�� | T2/�� | T2/�� |
| Ha2CO2 | 23.3 | 20.0 | 23.7 |
| HaCO2 | 18.5 | 20.0 | 20.8 |
| �¶� �ܽ�� | 10�� | 20�� | 30�� | 40�� |
| Ha2CO2 | 12.5g | 21.5g | 39.7g | 40��g |
| HaHCO2 | 8.1g | 9.6g | 11.1g | 12.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3.4 | B�� | 1��1.7 | C�� | 2.6��1 | D�� | 4.6��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
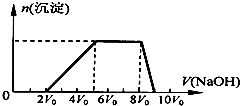 ij�����Һ�п��ܺ��е����������ʾ��
ij�����Һ�п��ܺ��е����������ʾ��| ���ܴ������е������� | H+��Ag+��Mg2+��Al3+��NH4+��Fe3+ |
| ���ܴ������е������� | Cl-��Br-��I-��CO32-��AlO2- |
| Cl2���������״���� | 5.6L | 11.2L | 22.4L |
| n ��Cl-�� | 2.5mol | 3.0mol | 4.0mol |
| n ��Br-�� | 3.0mol | 2.6mol | 1.6mol |
| n ��I-�� | x mol | 0 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
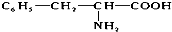 ����ͬ����ͬʱ�������������������ٱ����ϴ�������ȡ����������һ������ֱ�����ڱ����ϣ�����ϴ�������ͬ���칹����Ŀ�ǣ�������
����ͬ����ͬʱ�������������������ٱ����ϴ�������ȡ����������һ������ֱ�����ڱ����ϣ�����ϴ�������ͬ���칹����Ŀ�ǣ�������| A�� | 3 | B�� | 5 | C�� | 6 | D�� | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�2.54 g����ʱ������NaOH��Һ�������600 mL | |
| B�� | ��Ũ������HNO3�����ʵ���Ũ����14.0 mol/L | |
| C�� | NO2��N2O4 �Ļ�������У�NO2�����������80% | |
| D�� | �úϽ���ͭ��þ�����ʵ���֮����2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��أ��״�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
�й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��أ��״�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ�� �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com