
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点/℃ | 920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
| A、铝的化合物的晶体中,有的是离子晶体 |
| B、表中物质里只有BCl3和CO2的晶体是分子晶体 |
| C、同主族元素的氧化物可能形成不同类型的晶体 |
| D、不同主族元素的氧化物可能形成相同类型的晶体 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、Na+(g)+Cl-(g)═NaCl(s);△H | ||
B、Na(s)+
| ||
| C、Na(s)═Na(g);△H2 | ||
| D、Na(g)-e-═Na+ (g);△H |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图1 证明非金属性强弱:S>C>Si |
| B、图2 制备少量氧气 |
| C、图3 配制一定物质的量浓度的硫酸溶液 |
| D、图4 制备少量乙酸丁酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
| B、Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
| C、Cu2++H2S=CuS↓+2H+ |
| D、FeS+2H+=Fe2++H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡
在2L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 实 验 | 分离Na2CO3溶液和CH3CH2OH | 除去Cl2中含有的少量HCl | 做Cl2对NaOH溶液的喷泉实验 | 制取少量氨气 |
| 装 置 或 仪 器 | 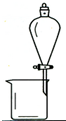 |  |  |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4溶液 |
| B、HBr溶液 |
| C、NaCl溶液 |
| D、硫酸溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com