
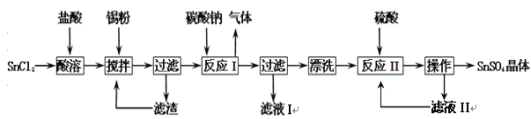
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易水解,易被氧化。某研究小组设计SnSO4制备路线如下:
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是 ;
(2)反应I得到的沉淀是SnO,得到该沉淀的离子方程式是 ;
(3)在反应I得到沉淀SnO后,要进行“过滤”、“漂洗”,检验SnO是否洗涤干净的操作是 ;
(4)反应II之后的“操作”依次为 、 、过滤、洗涤、低温干燥;
(5)某化学兴趣小组对用于微电子器件生产的锡粉进行了纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3溶液;③用0.2000 mol/L 酸性K2Cr2O7溶液滴定(产物中Cr呈+3价)至终点,消耗K2Cr2O7溶液15.00 mL。写出酸性K2Cr2O7溶液滴定的离子方程式 ,则此锡粉样品中锡的质量分数为__________________。
【答案】(1)抑制SnCl2水解 (2)Sn2++CO32-═SnO↓+CO2↑
(3)取最后一次洗涤后滤液少许于试管中,依次滴加足量硝酸、少量硝酸银溶液,观察到无白色沉淀;
(4)蒸发浓缩、冷却结晶;
(5)6Fe2++Cr2O72-+14H+ = 6Fe3++2Cr3++7H2O 90%
【解析】
试题分析:(1)SnCl2在水中发生水解反应:SnCl2+H2O═Sn(OH)Cl+HCl(可逆反应,应该用可逆号),生成难溶物Sn(OH)Cl,溶液含有杂质,若加入HCl,可使平衡向逆反应方向移动,抑制Sn2+水解;
(2)反应Ⅰ为向SnCl2溶液中加碳酸钠,得到的沉淀为SnO,反应离子方程式为Sn2++CO32-═SnO↓+CO2↑;
(3)沉淀SnO的表面附着液中含有氯离子,反复洗涤后,取最后一次洗涤后滤液少许于试管中,依次滴加足量硝酸、少量硝酸银溶液,观察到无白色沉淀,即可证明洗涤干净;
(4)通过蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥即可从反应II后的溶液中获得SnSO4晶体;
(5)Fe2(SO4)3将Sn2+全部氧化为Sn4+,再用溶液K2Cr2O7溶液滴定,将Fe2+氧化为Fe3+,其中酸性K2Cr2O7溶液氧化Fe2+的离子方程式为6Fe2++Cr2O72-+14H+ = 6Fe3++2Cr3++7H2O;
设粉中锡的质量分数为x,则:
3Sn~3Sn2+~6Fe3+~6Fe2+~K2Cr2O7
3×119g 1mol
1.19g×x 0.200mol/L×0.015L
故(3×119g):(1.19g×x)=1mol:(0.200mol/L×0.015L)
解得x=90%。


科目:高中化学 来源: 题型:
【题目】T0C时,在一个体积为2L的容器中,A气体和B气体反应反应生成C气体,反应过程中A、B、C浓度变化如图所示.
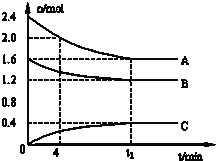
(1) 写出该反应的方程式:_______________
(2) 计算该温度下该反应的平衡常数:_______________
(3) 已知:K(300℃)>K(350℃),该反应是____________热反应.
(4) 0~4分钟时,B的平均反应速率为:_______________
(5) 到达平衡时A的转化率为:_______________
(6) 恒容条件下,下列措施中能使n(A)/n(C)降低的有____________.
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是:
A. 甲烷的标准燃烧热为890.3kJ.mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ.mol-1
B. CO(g)的燃烧热是283.0 kJ/mol ,则CO2(g)=2CO(g)+O2(g)的反应热△H=+2×283.0 kJ/mol
C. NaOH和HCl反应的中和热 △H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
D. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应3H2(g)+N2(g)![]() 2NH3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
2NH3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
A.增大压强 B.降低温度 C.使用高效催化剂 D.充入更多N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为( )
A. 0.05 mol B. 1 mol C. 1.05 mol D. 0.13 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,10mL 0.40mol·L-1H2O2溶液发生催化反应分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表.
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol﹒L-1﹒min-1
B.6~10min的平均反应速率:v(H202)<3.3×10-2mol﹒L-1min-1
C.反应至6min时,c(H2O2)=0.30mol﹒L-1
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制0.2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A.950mL,11.2g B.500mL,11.7g C.1000mL,11.7g D.任意规格,11.12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaOH溶液与CuSO4溶液加入某病人的尿液中,微热时如果观察到红色沉淀,则说明该病人的尿液中含有
A.乙酸 B.乙醇 C.氯化钠 D.葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com