
| A、锌与盐酸反应 |
| B、NaOH和HCl反应 |
| C、Ba(OH)2?8H2O与NH4Cl的反应 |
| D、CaCO3受热分解为CaO和CO2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 用甲装置制备并收集少量NO2气体 |
B、 通过乙装置实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
C、 装置丙可用于定量测定H2O2的分解速率 |
D、 装置丁可用于实验室制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
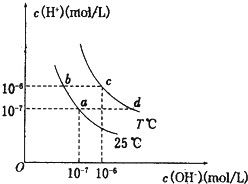 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )| A、c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Fe2+ |
| B、b点对应的溶液中大量存在:NH4+、K+、Cl-、NO3- |
| C、d点对应的溶液中大量存在:Al3+、K+、ClO-、Cl- |
| D、a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgX2 |
| B、Mg2X5 |
| C、Mg2X3 |
| D、Mg3X2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHS在水中的电离方程式为:NaHS═Na++HS-和HS-═H++S2- |
| B、同物质的量浓度的氨水和盐酸反应至中性时所用体积:V(NH3?H2O)>V(HCl) |
| C、Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)=c(OH-) |
| D、同浓度的下列溶液中,c(CH3COO-)的大小:CH3COONa>CH3COONH4>CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Li+、H+、NO3-、SO42- |
| B、Na+、Cu2+、OH-、SiO32- |
| C、NH4+、Al3+、Br-、AlO2- |
| D、Ba2+、K+、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜-锌-稀硫酸组成的原电池中,锌为正极 |
| B、铜-锌-稀硫酸组成的原电池中,电解质溶液的质量逐渐减轻 |
| C、用石墨电极电解CuCl2溶液时,阳极上Cu2+放电而析出金属铜 |
| D、用石墨电极电解CuCl2溶液时,电解质溶液的浓度逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | |
| 分类标准 | 含氧酸 | 分散系 | |
| 不属于该类别的物质 | Na2CO3 |
| 分类标准 | 能导电的物质 | 电解质 | 强电解质 |
| 属于该类的物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com