
【题目】A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示。已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质。(部分反应物、生成物及反应条件己略去)

请回答:
(1)写出B、D、F的化学式:B____,D____,F_____。
(2)写出B物质的一种用途_____,C与E反应的化学方程式是_________。
(3)图中物质相互间发生的反应。未涉及的基本反应类型是________。
【答案】CO2 H2SO4或者HNO3 H2O 灭火 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 置换反应
【解析】
A~F为初中化学常见的六种物质,且都含有一种相同元素,A、B、C、D、E是不同类别的物质,C俗称纯碱,所以C是碳酸钠,F是人体中含量最多的物质,所以F是水,A和水可以相互转化,所以A是氧气,氧气会转化成B,B和碳酸钠可以相互转化,所以B是二氧化碳,水会转化成E,E和碳酸钠会反应,所以E可以是氢氧化钙,氢氧化钙和碳酸钠都会与D反应,所以D可以是硫酸或硝酸,氧气和氢气会生成水,水通电会生成氢气和氧气,氧气和木炭会生成二氧化碳,二氧化碳和水会发生反应,水和氧化钙会生成氢氧化钙,二氧化碳和碳酸钠可以相互转化,碳酸钠、氢氧化钙都会与硫酸反应,推出的A~F中都含有氧元素,推导合理。
(1)B为CO2,D为H2SO4或者HNO3,F为H2O;
(2)B为CO2,它的用途可以是灭火等,C与E反应的化学方程式是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)图中物质相互间发生的反应,未涉及的基本反应类型是置换反应。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某烯烃与H2发生加成反应后得到的产物是CH3-CH(CH3)2.
(1)该产物的一氯代物有 _______________种;
(2)原来烯烃的结构简式为: _________________ ;
(3)该烯烃一定条件下发生加聚反应写出加聚产物的结构简式为:_________________;
(4)写出原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式:
_______________________________________________;
(5) 系统命名法的名称______________________。
系统命名法的名称______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F( )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:

已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②
请回答下列问题:
(1)X的化学名称是_________________。
(2)E生成F的反应类型为_________________。
(3)D的结构简式为_________________。
(4)由B生成C的化学方程式为_________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢普显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式___________、__________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料—聚甲基丙烯酸羟乙酯( )的合成路线(无机试剂自选):_________________。
)的合成路线(无机试剂自选):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某硫酸铜样品中硫酸铜的含量(杂质不溶于水,不含铜元素,不与其他物质发生反应),进行了如图实验:

(1)上述实验过程中发生反应的化学方程式为______。
(2)根据已知条件列出求解C烧杯中参加反应的硫酸铜质量(X)的比例式___。
(3)配制上述实验所用的氢氧化钾溶液,需要质量分数为40%的氢氧化钾溶液的质量为___。
(4)样品中硫酸铜的质量分数为___。
(5)D烧杯溶液中溶质的质量分数为____。
(6)若用湿法冶金的方法冶炼出100kg含杂质4%的铜,需要这种硫酸铜的质量为多少?(写出计算过程)____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线①代表滴定盐酸的曲线
B. 滴定醋酸的过程应该选择甲基橙作为指示剂
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol·L-1的NaOH溶液分别滴定同浓度、体积均为20.00mL的盐酸和醋酸溶液(用HA表示酸),得到2条滴定曲线,如图所示。
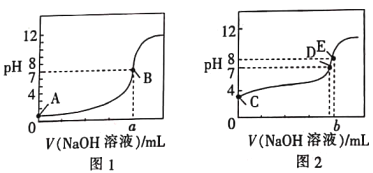
下列说法正确的是
A. 滴定醋酸的曲线是图1
B. 由图分析可得b>a=20
C. D点对应的溶液中:c(Na+)=c(A-)
D. 根据E点可计算得K(HA)=[0.05+(10-6-10-8)]×10-8/(10-6-10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发射“神舟七号”载人飞船的是我国自行研制的“长征一号D”运载火箭。该火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A. 此反应是氧化还原反应
B. 反应瞬间产生大量高温气体,推动火箭飞行
C. 在此反应中![]() 作还原剂
作还原剂
D. R的分子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中要配制0.1mol/L 盐酸500mL。请回答下列问题:
(1)实验中用到仪器除量筒、烧杯、玻璃棒外还需用的仪器有:____________________;
(2)实验中应用量筒量取密度为1.19 g/cm3、质量分数为36.5%的浓盐酸_______ mL;
(3)下列操作能引起所配溶液浓度偏高的是_____________ 。
A.取浓盐酸时俯视
B.将浓盐倒出后,洗涤量筒,并将洗涤液倒入烧杯中
C.将稀释后的盐酸转移后,直接加水定容至刻度线
D.定容时俯视
E. 颠倒摇匀后发现液面低于刻度线,但未加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com