
 ��ͼ��ij��ѧѧϰС������̽������ˮ��Ӧ��ʵ��װ�ã���װ�ÿ��Լ���Ӧ���ռ�������������һ�壮ͼ���ƿ����ô�ͷ���ס�ģ�����գ�
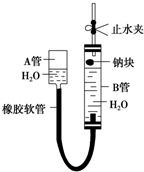
��ͼ��ij��ѧѧϰС������̽������ˮ��Ӧ��ʵ��װ�ã���װ�ÿ��Լ���Ӧ���ռ�������������һ�壮ͼ���ƿ����ô�ͷ���ס�ģ�����գ����� ��1���˷�Ӧԭ��Ϊ����ˮ�ķ�Ӧ�����ƿ���ˮ�Ӵ�����������AB���������ͨ�����ҵ���A�ܸ߶ȿ�����ʱ�����ƿ���ˮ�Ƿ�Ӵ����ݴ˽�ɣ�
��2������ˮ��Ӧ�����������ƺ��������ݴ���д��ѧ��Ӧ����ʽ��
��3����ȼ�����ȼǰ����Ҫ�����䴿�ȣ����ڴ�װ��B���Ϸ����Ե���ˮ�ĸ߶��ų�װ���ڵĿ���������ȡ�������Ǵ����ģ�������ȼ����ˮ��
��� �⣺��1������ˮ�ķ�Ӧ�����ƿ���ˮ�Ӵ�����������AB���������ͨ�����ҵ���A�ܸ߶ȿ�����ʱ�����ƿ���ˮ�Ƿ�Ӵ���������A��ʱ������Ӧ��ֹˮ�У���������ѹ��ͨ��Ȼ������ ����A�ܣ��Ա���B����ˮ��������B�����ƿ���ˮ�Ӵ�ʱ��Ϊ�������������Ӧ�ر�ֹˮ�У���A�ܵ������ǣ�����ˮ��߶��Կ����ƿ���ˮ�ĽӴ���
�ʴ�Ϊ�������� ����A�ܣ��رգ�����ˮ��߶��Կ����ƿ���ˮ�ĽӴ���
����2������ˮ��Ӧ�����������ƺ����������ӷ�Ӧ����ʽΪ��2Na+2H2O�T2Na++2OH-+H2����
�ʴ�Ϊ��2Na+2H2O�T2Na++2OH-+H2����
��3����ȼ�����ȼǰ����Ҫ�����䴿�ȣ����ڴ�װ��B���Ϸ����Ե���ˮ�ĸ߶��ų�װ���ڵĿ���������ȡ�������Ǵ����ģ���ȼ��ʵ���в���������IJ����������������������ܿڣ�Ȼ���ֹˮ�У�������ȼ����ˮ����ѧ��Ӧ����ʽΪ��2H2+O2$\frac{\underline{\;��ȼ\;}}{\;}$2H2O��
�ʴ�Ϊ�����������Ĵ��ȣ��ռ����������Ǵ����ģ��������������ܿڣ�Ȼ���ֹˮ�У�2H2+O2$\frac{\underline{\;��ȼ\;}}{\;}$2H2O��
���� ������Ҫ�����������ˮ�ķ�Ӧ���漰ʵ�����������ʵ��ԭ����������ѧ��Ӧ����ʽ����д�ȣ��ѶȲ����ܿ���ѧ��������ѧ��ѧ֪ʶ�ۺϷ����ͽ��ʵ�������������������ѧ�����������˼ά��ȣ�ǿ����ѧ������֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
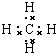 ���ռ乹�����������壬����Ľṹ��ʽΪCH3CH2CH3���춡��Ľṹ��ʽ��CH3��2CH2CH3��
���ռ乹�����������壬����Ľṹ��ʽΪCH3CH2CH3���춡��Ľṹ��ʽ��CH3��2CH2CH3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
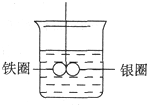 ��ͼ��ʾ����ʢ��ˮ���ձ��У���Ȧ����Ȧ�����Ӵ�����һ����Ե��ϸ˿��ʹ֮ƽ�⣮С�ĵش��ձ��������CuSO4��Һ��
��ͼ��ʾ����ʢ��ˮ���ձ��У���Ȧ����Ȧ�����Ӵ�����һ����Ե��ϸ˿��ʹ֮ƽ�⣮С�ĵش��ձ��������CuSO4��Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
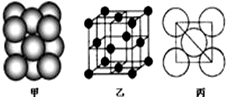
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 �����к��еĻ�ѧ�������ǣ����ԣ����ۼ�
�����к��еĻ�ѧ�������ǣ����ԣ����ۼ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com