
【题目】下列物质的转化在给定条件下能实现的是( ) ①NaAlO2(aq) ![]() AlCl3
AlCl3 ![]() Al
Al
②NH3 ![]() NO
NO ![]() HNO3
HNO3
③NaCl(饱和) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④FeS2 ![]() SO3
SO3 ![]() H2SO4 .
H2SO4 .
A.②③
B.①④
C.②④
D.③④
【答案】A
【解析】解:①氯化铝固体是共价化合物,由分子构成,无离子,无法电解,所以得不到铝,故①错误;②氨气的催化氧化会生成一氧化氮,一氧化氮易被氧化为二氧化氮,二氧化氮溶于水中得到硝酸,故②正确;
③在饱和食盐水中通入氨气,形成饱和氨盐水,再向其中通入二氧化碳,在溶液中就有了大量的钠离子、铵根离子、氯离子和碳酸氢根离子,其中NaHCO3溶解度最小,析出NaHCO3 , 加热NaHCO3分解生成碳酸钠,故③正确;
④FeS2和氧气反应生成二氧化硫,不能直接生成三氧化硫,故④错误;
故选A.
【考点精析】认真审题,首先需要了解氨的化学性质(与水反应,NH3是惟一能使润湿的红色石蕊试纸交蓝的气体,常用此性质检验NH3;与酸反应:NH3+HCl=NH4Cl(生成白烟);与O2反应:4NH3+5O2=4NO+6H2O+Q;


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 6.02×1023是阿伏加德罗常数的近似值
B. 阿伏加德常数个微粒的物质的量是1mol
C. 1mol12C原子的质量为12g
D. 硫酸的摩尔质量是98克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
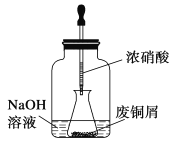
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________________。
(2)上图装置中NaOH溶液的作用是_________________________。
(3)步骤二中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外),水浴加热的优点是_______________________。
(4) 已知:CuCO3、Cu(OH)2受热均易分解,产物中都有CuO生成。碱式碳酸铜可表示为xCuCO3·yCu(OH)2·zH2O(x、y、z取整数),测定碱式碳酸铜组成的方法有多种,现采用氢气还原法,请回答如下问题:(已知M(Cu)=63.5 g·mol-1)。
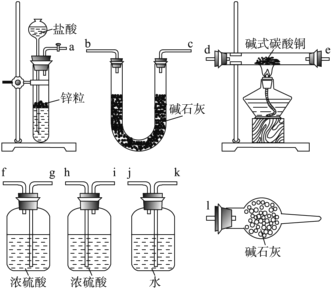
①写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式:__________________;
②实验装置用上面所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):( a )→( )( )→( )( )→( )( )→( )( )→( )( )→( l )_____
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为______ g,化学式为____________。
④某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?__________(填“可行”或“不可行”)请说明理由________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】限用硫酸、盐酸、醋酸、钠盐、钾盐在溶液中反应,符合离子方程式2H++CO32-===H2O+CO2↑的化学方程式的个数有( )
A. 3B. 5C. 8D. 12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示.下列说法错误的是( ) 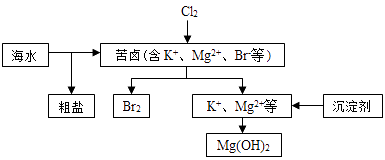
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请按要求回答有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | … | |||||||
2 | … | ② | ③ | ④ | |||||
3 | ⑤ | … | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | … | ⑩ |
(1)④、⑤、⑥的原子半径由大到小的顺序是________(用元素符号表示)
(2)②、⑦两种元素最高价氧化物对应的水化物中酸性最强的是 ______(用化学名称表示),能证明以上结论的化学方程式是 ______________________________________
(3)第三周期元素形成的简单离子中半径最小的微粒是_____(用离子符号表示),写出⑥元素的单质与⑤最高价氧化物对应的水化物反应的离子方程式____________________。
(4)元素③、⑧的氢化物中,沸点较低的物质的结构式是_____; 请简述理由_______________。
(5)①、③、④、⑥元素可形成含10个电子的微粒,其中A和B为分子,C和E为阳离子,D为阴离子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。用电子式表示下列4种微粒。
A________、B________、C________、D________。
(6)⑨元素与⑩元素两者核电荷数之差是 ____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液中粒子浓度的关系式正确的是( )
A.25℃,0.1mol/L pH=4.5 的NaHC2O4溶液 c(HC2O ![]() )>c(C2O
)>c(C2O ![]() )>c(H2C2O4)
)>c(H2C2O4)
B.向0.2mol/L的NaHCO3溶液中加入等体积的0.1mol/L的NaOH溶液c(H+)+c(Na+)=c(OH﹣)+c(CO ![]() )+c(HCO3﹣)
)+c(HCO3﹣)
C.常温下,氯化铵和氨水的混合溶液其pH=7,c(Cl﹣)=0.1mol/L c(Cl﹣)>c(NH4+)>c(OH﹣)=c(H+)
D.浓度均为0.1mol/L的醋酸钠和醋酸的混合溶液中c(CH3COO﹣)﹣c(CH3COOH)=2[c(H+)﹣c(OH﹣)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于 Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ΔH <0 的化学反应,下列 叙述错误的是
A. 反应过程中能量关系可用下图表示

B. 若将该反应设计成原电池则锌为负极
C. ΔH 的值与反应方程式的化学计量数有关
D. 若将其设计为原电池,当有 32.5g 锌溶解时,正极放出气体一定为 11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,有pH均为9体积均为10mL的NaOH溶液和CH3COONa溶液,下列说法正确的是( )
A.两种溶液中的c(Na+)相等
B.两溶液中由水电离出的c(OH﹣)之比为 ![]()
C.分别加水稀释到100mL时,两种溶液的pH依然相等
D.分别与同浓度的盐酸反应,恰好反应时消耗的盐酸体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com