
����Ŀ����������̼�ܵ��о��ɹ������˿Ƽ��Ľ��������õ绡���ϳɵ�̼���ܳ����д�������������̼������������̼���������������������ᴿ�䷴ӦʽΪC��K2Cr2O7��H2SO4��CO2��K2SO4��Cr2(SO4)3��H2O��δ��ƽ��
��1����ƽ��������ʽ__C��__K2Cr2O7��__H2SO4��__CO2�� __K2SO4��__Cr2(SO4)3��__H2O
��2��������Ӧ����������_______���ѧʽ��������������__________���ѧʽ��
��3��H2SO4��������Ӧ�б��ֳ�����������_______������ţ�
a.������ b.�����Ժ����� c.���� d.��ԭ�Ժ�����
��4������Ӧ�е���ת����0.8mol��������������ڱ�״���µ����Ϊ__________ L
��5��Ҫʹ10mL0.5mol/L��K2Cr2O7����Һ����ԭ������Ҫ���� ________ mL2mol/L��H2SO4��Һ
���𰸡�3 2 8 3 2 2 8 K2Cr2O7 CO2 c 4.48 10
��������
��1��̼Ԫ�ػ��ϼ���0����Ϊ+4��CrԪ�ػ��ϼ���+6����Ϊ+3�����ݵ�ʧ�����غ㡢Ԫ���غ���ƽ��
��2������Ԫ�ػ��ϼ۽��͵ķ�Ӧ��������������ԭ��ʧ���ӻ��ϼ����ߵõ��IJ������������
��3��H2SO4��Ԫ�ػ��ϼ۲��䣬����K2SO4��Cr2(SO4)3���ɣ�
��4���� ��֪������3mol CO2ת��12mol���ӡ�
��֪������3mol CO2ת��12mol���ӡ�
��5�����ݻ�ѧ����ʽ����Ҫʹ10mL0.5mol/L��K2Cr2O7��Һ����ԭ����Ҫ2mol/L��H2SO4��Һ�������
��1��̼Ԫ�ػ��ϼ���0����Ϊ+4��CrԪ�ػ��ϼ���+6����Ϊ+3�����ݵ�ʧ�����غ㡢Ԫ���غ���ƽ����ʽΪ3C��2K2Cr2O7��8H2SO4��3CO2��2K2SO4��2Cr2(SO4)3��8H2O
��2������Ԫ�ػ��ϼ۽��͵ķ�Ӧ������������CrԪ�ػ��ϼ���+6����Ϊ+3������K2Cr2O7 ������������ԭ��ʧ���ӻ��ϼ����ߵõ��IJ������������CԪ�ػ��ϼ���0����Ϊ+4������������CO2��
��3��H2SO4��Ԫ�ػ��ϼ۲��䣬����K2SO4��Cr2(SO4)3���ɣ�������ֳ��������������ԣ���ѡc��
��4���� ��֪������3mol CO2ת��12mol���ӣ�����ת��0.8mol��������CO2�����ʵ�����
��֪������3mol CO2ת��12mol���ӣ�����ת��0.8mol��������CO2�����ʵ�����![]() ��������������ڱ�״���µ����Ϊ0.2mol��22.4L/mol=4.48 L��
��������������ڱ�״���µ����Ϊ0.2mol��22.4L/mol=4.48 L��
��5������Ҫ2mol/L��H2SO4��Һ�����ΪVL��
3C��2K2Cr2O7��8H2SO4��3CO2��2K2SO4��2Cr2(SO4)3��8H2O
2 8
0.01L��0.5mol/L V��2mol/L
![]()
V=0.01L=10 mL



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йؾ���Ľṹ��ͼ��ʾ������˵��������ȷ���� (����)


A. ��NaCl����������Na�������Cl�����������
B. ��CaF2��������ÿ������ƽ��ռ��4��Ca2��
C. �ڽ��ʯ��������̼ԭ����̼̼�������ı�Ϊ1��2
D. ����̬�Ŵط��ӵķ���ʽΪEF��FE
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þһ������صĹ���ԭ����ͼ��ʾ����ط�Ӧ����ʽΪ��2Mg+O2+2H2O=2Mg(OH)2���йظõ�ص�˵����ȷ���ǣ� ��
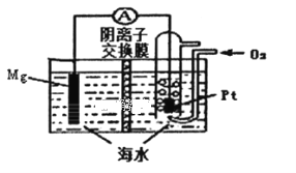
A. ͨ�������ĵ缫Ϊ����
B. ��ع���ʱ����Һ�е�Na+�ɸ�����������
C. �����ĵ缫��ӦΪMg-2e-+2OH-=Mg(OH)2
D. ����·��ת��0.04 mol����ʱ���μӷ�Ӧ��O2Ϊ���224ml
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦmA(s)+nB(g)![]() eC(g)+fD(g)����Ӧ�����У���������������ʱ��C�����������(C)�ڲ�ͬ�¶ȺͲ�ͬѹǿ����������ʱ��ı仯��ͼ��ʾ��
eC(g)+fD(g)����Ӧ�����У���������������ʱ��C�����������(C)�ڲ�ͬ�¶ȺͲ�ͬѹǿ����������ʱ��ı仯��ͼ��ʾ��
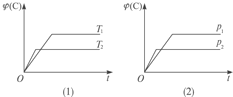
����������ȷ����()
A. ƽ�����ʹ�ô�����C�������������
B. ƽ������¶����ߣ���ѧƽ��������Ӧ�����ƶ�
C. ��ѧ����ʽ�У���ѧ�������Ĺ�ϵΪn<e��f
D. ƽ�������A����������ѧƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������Ũ�Ⱦ�Ϊ0.1 mol��L��1�����и���Һ��pH���±���ʾ�������й�˵����ȷ����(����)
���� | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A. ����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��H2CO3��HClO��HF
B. ����CO2ͨ��0.1 mol��L��1 Na2CO3��Һ������Һ�����ԣ�����Һ��2c(CO32��)��c(HCO3��)��0.1 mol��L��1(������Һ����仯)
C. �����ϱ���ˮ�ⷽ��ʽClO����H2O![]() HClO��OH����ƽ�ⳣ��K��10��7.6
HClO��OH����ƽ�ⳣ��K��10��7.6
D. ������NaClO��Һ��ͨ����CO2��������ӷ���ʽΪ��2ClO����CO2+H2O === 2HClO��CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA ��ʾ�����ӵ�������ֵ��������������ȷ����
A. ���³�ѹ�£�17g ��(��14CH3)������������Ϊ 9 NA
B. ��⾫��ͭ�Ĺ����У����������� 64 g�����·��һ��ͨ�� 2NA ������
C. NA �� Fe(OH)3 �������ӵ�����Ϊ 107 g
D. 1mol ͭ��������������Ӧ��ת�Ƶ�����Ϊ NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾʵ����ijŨ�����Լ�ƿ�ϵı�ǩ���Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺

��1����Ũ��������ʵ���Ũ��Ϊ___mol��L��1��
��2��ȡ����������ĸ�Ũ����ʱ�������������в�����ȡ����Ķ��ٶ��仯����__(����ĸ����)��
A.��Һ��HCl�����ʵ��� B.��Һ��Ũ�� C.��Һ��Cl������Ŀ D.��Һ���ܶ�
��3��ijѧ����������Ũ���������ˮ����480mL���ʵ���Ũ��Ϊ0.400mol��L��1��ϡ���ᡣ
�ٸ�ѧ����Ҫ��ȡ__mL������һλС��������Ũ����������ơ����ʵ������5mL��10mL��20mL��Ͳ��Ӧѡ��__mL��Ͳ��á�����ȡʱ������Ͳ���ɾ�����ˮϴ����ֱ����ȡ��������ҺŨ�Ƚ�___(ƫ�ߡ�ƫ�͡���Ӱ��)��
������ʱ��������������Ͳ�⣬����Ҫ�������У�___��
����������ᵼ��������Һ��Ũ��ƫ�͵���__(����ĸ����)��
A.Ũ����ӷ���Ũ�Ȳ��� B.����ǰ����ƿ����������ˮ
C.������Һʱ����������ƿ�̶��� D.��ˮʱ�����̶��ߣ��ý�ͷ�ι�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������н��з�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.4mol/L��0.2mol/L��0.4mol/L������Ӧ��ƽ��ʱ�����ܴ��ڵ�������
2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.4mol/L��0.2mol/L��0.4mol/L������Ӧ��ƽ��ʱ�����ܴ��ڵ�������
A. SO2Ϊ0.8mol/L��O2Ϊ0.4mol/L
B. SO2Ϊ0.5mol/L
C. SO3Ϊ0.8mol/L
D. SO2��SO3һ����Ϊ0.3mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ��ϡ���ᷴӦ�Ʊ�NO�ǻ�ѧʵ���ѧ�е���Ҫʵ��֮һ���������ڷ�Ӧ���Ȳ����ơ�NO�ױ������Լ�������ɿ�����Ⱦ��ԭ���ڽ�ѧʵ���в��ײ�������ͼΪ��ʵ����иĽ�ʾ��ͼ���ش��������⣺

��1����װʵ��װ�ò�����װ�õ������ԣ����������Եķ���Ϊ___��
��2�������װ�����������ã���ͼװ��ҩƷ�����ܱ�֤B�е��������������ܴ������ϸ��壬Ȼ�������ϸ���������ͭƬ���ڷ�Ӧ����ǰ��Ҫ���еı�Ҫ����Ϊ�����Թ�C�ϲ���ֹˮ�У���A��ͨ��__���壬��__ʱ��ֹͣ��A��ͨ���壬����ֹˮ�м�סA�ڵ��ܡ�
��3������Cu��ϡHNO3��Ӧ�����IJ�����__��
��4��B�е�ʵ������___��
��5������ʹʵ��ֹͣ�IJ�����___��
��6��ʵ����ɫ����Ѹ�ٱ�Ϊ����ɫ�IJ�����____��
��7������ʯ��ˮ��պ��NaOH��Һ�����Ŷ���������β������NaOH��Һ����NO��NO2��������������ʣ�࣬��д��������Ӧ�����ӷ���ʽ��___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com