
【题目】回答有关氯气制备的几个问题
实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有两个同学分别设计的两套实验装罝如下图:
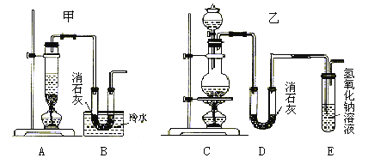
(1)写出制取氯气的离子方程式_______________________________。
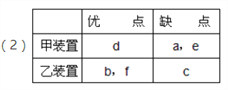
(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染坏境。
优 点 | 缺点 | |
甲装罝 | ________ | ________ |
乙装罝 | ________ | ________ |
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,请从上述装罝中选取合理的部分,组装一套较完整的实验装罝,装置各部分连接顺序是(按气流流动的方向)__________。该组合中还缺少的装罝是_____________,原因是__________________________________。
(4)实验室若用16mol/L的盐酸l00mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过__________ mol。
【答案】 MnO2+4H++ 2CI(浓)![]() Mn2++Cl2↑+2H2O d a,e b,f c C、B、E 还缺少除去氯气中的氯化氢杂质的装置 因为氯化氢可以与Ca(OH)2和Ca(ClO)2反应 0.2
Mn2++Cl2↑+2H2O d a,e b,f c C、B、E 还缺少除去氯气中的氯化氢杂质的装置 因为氯化氢可以与Ca(OH)2和Ca(ClO)2反应 0.2
【解析】本题分析:本题主要考查对于“氯气和Ca(OH)2制取少量漂白粉”实验的评价。
(1)制取氯气的离子方程式为MnO2+4H++ 2CI(浓)![]() Mn2++Cl2↑+2H2O 。
Mn2++Cl2↑+2H2O 。
(3)装置各部分连接顺序是CBE。该组合中还缺少的装罝是除去氯气中的氯化氢杂质的装置,原因是因为氯化氢可以与Ca(OH)2和Ca(ClO)2反应。
(4)HCl的物质的量为n=cV=16mol/L×0.1L=1.6mol,8HCl~2Cl2~Ca(C1O)2,次氯酸钙的物质的量最多不超过0.2 mol。


科目:高中化学 来源: 题型:
【题目】已知化学反应 A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是
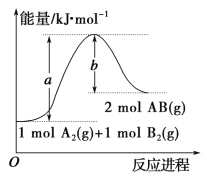
A.每生成2分子AB 吸收 b kJ 热量
B.该反应热 ΔH=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂 1 mol A—A 和1 mol B—B 键,放出 a kJ 能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在以下各种情形下,下列电离方程式的书写正确的是
A.熔融状态下的NaHSO4电离:NaHSO4=Na++H++SO42-
B.H2CO3的电离:H2CO3![]() 2H++CO32-
2H++CO32-
C.Fe(OH)3的电离:Fe(OH)3![]() Fe3++3OH-
Fe3++3OH-
D.水溶液中的NaHSO4电离:NaHSO4=Na++HSO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下在密闭容器中发生如下反应:2M(g)+N(g) ![]() 2E(g)若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为
2E(g)若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为
A.20% B.40% C.60% D.80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离方法错误的是
A.采用蒸发法从食盐水中提取食盐
B.用结晶法除去硝酸钾中的氯化钠
C.用酒精从溴水中萃取溴
D.用分液法分离汽油和水的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如下图,其中只有M为金属元素。下列说法不正确的是( )
![]()
A. 原子半径Z < M
B. Y的最高价氧化物对应水化物的酸性比X 的弱
C. X 的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第二周期第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是( )
A. Al3+、Na+、HCO3-、OH- B. Na+、Fe2+、H+、NO3-
C. K+、Fe3+、SCN-、SO32- D. Na+、Ag+、H+、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com