
【题目】气态烃X在标准状态下的密度为1.16gL-1,D能发生银镜反应,E为聚氯乙烯,有关物质的转化关系如下:请回答下列问题:
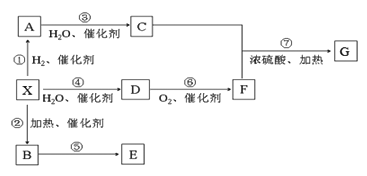
(1)反应②的反应类型为_____________,一定条件下X能发生类似于⑤的反应,
所得高分子化合物的结构简式为_________________。
(2)A与F在催化剂作用下直接生成G的化学方程式为___________________________。
(3)下列说法正确的是_________。
A.A、B、E均能使酸性高锰酸钾溶液褪色
B.G的同分异构体中能与碳酸氢钠反应生成CO2气体的物质有4种
C.F、G都能与NaOH溶液反应,且都生成钠盐
D.X先后与F、H2反应也可以制得G
【答案】 加成反应 ![]()
![]() CD
CD
【解析】试题分析:气态烃X在标准状态下的密度为1.16gL-1,X的摩尔质量为1.16gL-1×22.4L/mol=26g/mol,所以X是乙炔;D能发生银镜反应,则D是乙醛;根据流程图F是乙酸;结合X、C可知A是乙烯,C是乙醇;乙酸、乙醇在浓硫酸条件下发生反应生成乙酸乙酯,所以G是乙酸乙酯;E为聚氯乙烯,B是氯乙烯。
解析:根据以上分析,(1)乙炔与氯化氢反应生成氯乙烯的反应类型为加成反应,一定条件下乙炔发生加聚反应生成聚乙炔,聚乙炔的结构简式为![]() 。
。
(2)乙炔与乙酸在催化剂作用下直接生成乙酸乙酯的化学方程式为![]() 。
。
(3)聚氯乙烯变化双键,不能使酸性高锰酸钾溶液褪色,故A错误;
乙酸乙酯的同分异构体中能与碳酸氢钠反应生成CO2气体的物质属于酸,有CH3CH2CH2COOH、(CH3)2CHCOOH,共2种,故B错误;
乙酸、乙酸乙酯都能与NaOH溶液反应,且都生成乙酸钠,故C正确;
乙烯先与乙酸反应再与氢气加成生成乙酸乙酯,故D正确。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,写出其化学方程式_________________。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
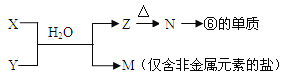
X溶液与Y溶液反应的离子方程式为_______________________________,
N→⑥的单质的化学方程式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁(FeTiO3),其中一部分Fe2+在风化过程中会转化为+3价。

已知:TiO(OH)2(即H2TiO3)为两性氢氧化物
(1)步骤②中,发生反应的主要离子方程式为______________。
(2)步骤③中,实现混合物的分离是利用物质的____________(填字母序号)。
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是____________(填操作名称)。
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:__________________________。
(5)上述工艺流程中可以循环利用的物质是____________。
(6)研究发现,可以用石墨作阳极、铁网作阴极、熔触CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。

①写出阳极所发生反应的电极反应式_________________________。
②在制备金属Ti前后,CaO的质量将______(填“增大”、“不变”或“减小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是
A. 稀Na2SO4溶液 B. 稀HCl溶液
C. CuCl2溶液 D. AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的每个编号代表一种元素。请根据要求回答问题:
| ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ② | ||||||||
3 | ③ | ④ | ⑤ | ⑥ | |||||
(1)①的原子序数是____________________;
(2)②、⑤两种元素形成的简单气态氢化物,较稳定的是________________(化学式);
(3)③、④两种元素相比较,原子半径较大的是_________(填元素符号);
(4)写出①与⑥两种元素所形成化合物的电子式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯、乙醇和乙酸是重要有机化合物,请根据题意填空:
(1)乙酸分子中含有的官能团名称是_______________;
(2)乙烯__________使溴水溶液褪色(填“能”或“不能”);
(3)乙醇跟乙酸在浓硫酸催化且加热的条件下发生反应,请完成化学方程式:
CH3COOH + CH3CH2OH ![]() CH3COOCH2CH3 + __________________
CH3COOCH2CH3 + __________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作能达到实验目的或不影响实验的是
A. 容量瓶用水洗净后,可不经干燥直接用于配制溶液
B. 向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体
C. 向溶液中滴加盐酸酸化的氯化钡,若有白色沉淀,说明溶液中含硫酸根
D. 蒸馏时应先加热然后再通冷凝水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com