
【题目】某气体MO2在20℃、1.013x105 Pa的条件下,对氢气的相对密度是23,则M的相对原子质量是( )
A.12B.14C.28D.32
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,产生1.16g白色沉淀。再向所得悬浊液中逐滴加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。试回答:
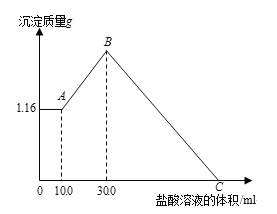
(1)写出A点到B点发生反应的离子方程式
(2)C点加入盐酸溶液的体积为 。
(3)原混合物中MgCl2的物质的量是 ,NaOH的质量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于单质硫的叙述中正确的是( )
A.硫的活泼性不如氯气
B.硫在过量纯氧中的燃烧产物是三氧化硫
C.硫与金属单质或非金属单质反应均做氧化剂
D.硫与铁反应产物为Fe2S3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)实验室模拟合成氨和氨催化氧化的流程如下:


(1)N元素在周期表中位置_______________________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有______________作用。
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是_______________________________________。
(4)写出乙装置中氨氧化的化学方程式:__________________________________________。
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。

请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是_______________________。
(6)实验过程中,装置丙中出现的现象是:________________________________________。
(7)装置丙中的试管内发生反应的离子方程式为:__________________________________。
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为______________色。
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应生成三种含氯盐: 0.7molKCl、0.2molKClO和X。则X是
A. 0.1molKClO4 B. 0.1molKClO3
C. 0.2molKClO2 D. 0.1molKClO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:
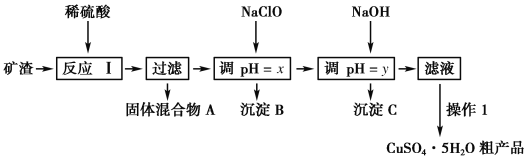
已知:①Cu2O+2H+===Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是____________ (写两条)。
(2)固体混合物A中的成分是________。
(3)反应Ⅰ完成后,铁元素的存在形式为________(填离子符号);写出生成该离子的离子方程式____________。
(4)操作1主要包括:蒸发浓缩、冷却结晶、________。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是______________。
(5)用NaCl0调pH可以生成沉淀B,利用题中所给信息分析沉淀B为_______,该反应的离子方程式为______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
A. 该反应的平衡常数表达式为K=c(CO)/c(CO2)
B. 该反应的逆反应是放热反应
C. v正(CO2)=v逆(CO)时该反应达到平衡状态
D. c(CO2):c(CO)=1:1时该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)硼、铟与镓同是ⅢA族元素,写出镓元素基态原子的价电子排布图:_______________。B3N3H6可用来制造具有耐油、耐高温性能的特殊材料,它的一种等电子体的分子式为_________,B3N3H6分子中N、B原子的杂化方式分别为_________、______。
(2)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、磷化镓及铜铟硒薄膜电池等。其中元素As、S、P、Ga的电负性由小到大的顺序为:______________________________________________。
(3)铜离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。某化合物Y与Cu(Ⅰ)(Ⅰ表示化合价为+1)结合形成图甲所示的离子。该离子中含有化学键的类型有____________________(填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
(4)向氯化铜溶液中通入足量的二氧化硫,生成白色沉淀M, M的晶胞结构如图乙所示。写出该反应的离子方程式:________________________________________________。
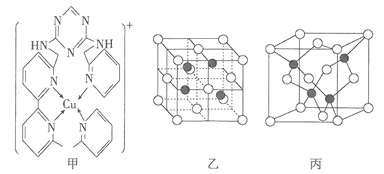
(5)已知由砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其晶胞结构如图丙所示,请写出化合物A的化学式_____________。设化合物A的晶胞边长为![]() pm,则每立方厘米该晶体中所含砷元素的质量为____________________g(NA表示阿伏加德罗常数的值)。
pm,则每立方厘米该晶体中所含砷元素的质量为____________________g(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com