
| A、原子半径为D>C>A>B |
| B、原子序数为a>b>c>d |
| C、离子半径为A->B2->C+>D2+ |
| D、a+2=c |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、①②⑤ | B、②⑤⑦ |
| C、⑦⑧ | D、只有⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H2 C2H6 |
| B、CH4 C3H8 |
| C、C3H6 C3H6O2 |
| D、C2H4 C2H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核电荷数为3的元素 |
| B、核电荷数为18的元素 |
| C、核电荷数为6的元素 |
| D、核电荷数为16的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x、y的离子具有相同的电子层结构 |
| B、x-和y2-具有相同的电子层结构 |
| C、x+和y2-具有相同的电子层结构 |
| D、x-比y2-少一个电子层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
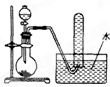
| A、用双氧水与二氧化锰反应制取O2 |
| B、用浓盐酸和MnO2反应制取Cl2 |
| C、用浓氨水和烧碱反应制取NH3 |
| D、用Na2SO3与硫酸反应制取SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com