
| 催化剂 |
| △ |
| A、只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B、该反应达到平衡后,反应就完全停止了,即正逆反应速率为零 |
| C、若用18O原子组成的O2参加反应,平衡时SO2中也会含有18O |
| D、在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |


科目:高中化学 来源: 题型:
| A、证明SO2具有强氧化性和酸性 | ||
| B、若第1支试管改通H2S或Cl2气体,后再通SO2气体,均不会产生沉淀 | ||
| C、若第2支试管改通NH3,后通SO2,不会产生沉淀 | ||
D、升高pH使SO2水溶液中SO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16g CH4含有的氢原子数为4NA |
| B、1mol羟基(-OH)含有10NA个电子 |
| C、1mol?L-1NaOH溶液中含有的钠离子为NA |
| D、标准状况下,33.6L CH3CH2OH 中含有的分子数目为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O+H2O═2NaOH | ||||
| B、CuSO4+Fe═Cu+FeSO4 | ||||
| C、K2CO3+2HCl═2KCl+H2O+CO2↑ | ||||
D、NH4Cl
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、邻二甲苯没有同分异构说明苯不是单双键交替 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、乙烯和苯都能使溴水褪色,褪色的原理相同 |
| D、乙醇、乙酸、苯都能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
D、苯酚钠溶液中通入少量CO2:2 -O-+CO2+H2O=2 -O-+CO2+H2O=2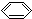 -OH+CO32- -OH+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 物质的化学式 | 浓H2SO4 | CCl4 | P4 | NH4NO3 |
| 危险警告标签 | 腐蚀品 | 易燃品 | 剧毒品 | 爆炸品 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用NH3表示的化学反应速率为0.1 mol/(L?s) |
| B、维持容积的体积不变充入氩气,会加快该反应的速率 |
| C、增加H2的浓度该正反应速率和逆反应速率都会加快 |
| D、反应足够长时间,N2、H2中至少有一种物质浓度降为零 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com