
A£® | B£®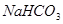 | C£®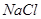 | D£®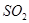 |
 ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø Ó¢²Å¼Ę»®ĘŚÄ©µ÷ŃŠĻµĮŠ“š°ø
Ó¢²Å¼Ę»®ĘŚÄ©µ÷ŃŠĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ü | B£®¢Ł¢Ż | C£®¢Ū¢Ü | D£®¢Ł¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NaŗĶO2 | B£®NaOHŗĶCO2 | C£®NaHCO3ÓėŃĪĖį | D£®MnO2ÓėŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ö»ÓŠ¢Ł¢Ś¢Ū | B£®Ö»ÓŠ¢Ł¢Ū¢Ü | C£®Ö»ÓŠ¢Ś¢Ū¢Ü | D£®¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| A£®ÓŠĘųĢåÉś³É | B£®ÄĘČŚ»Æ³ÉŠ”Ēņ²¢ŌŚŅŗĆęÉĻÓĪ¶Æ |
| C£®ČÜŅŗµ×²æÓŠŅų°×É«µÄ½šŹōøĘÉś³É | D£®ČÜŅŗ±ä»ė×Ē |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
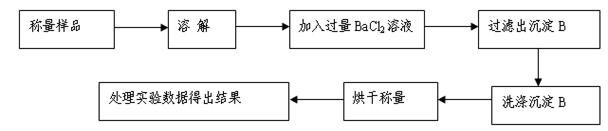
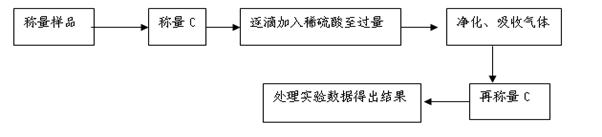

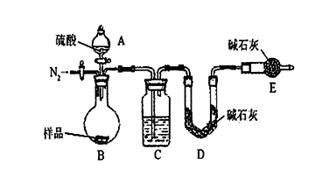
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| µĪ¶Ø“ĪŹż | “ż²āŅŗ£ØmL£© | 0.6000mol/LŃĪĖįČÜŅŗµÄĢå»ż£ØmL£© | |
| ³õ¶ĮŹż | ÖÕ¶ĮŹż | ||
| µŚŅ»“Ī | 20.00 | 1.00 | 21.00 |
| µŚ¶ž“Ī | 20.00 | ČēÓŅĶ¼¢ń | ČēÓŅĶ¼¢ņ |
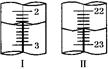 ĻŌŹ¾ĻūŗĵÄŃĪĖįČÜŅŗĢå»żĪŖ ”£
ĻŌŹ¾ĻūŗĵÄŃĪĖįČÜŅŗĢå»żĪŖ ”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
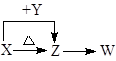
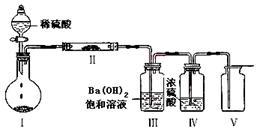
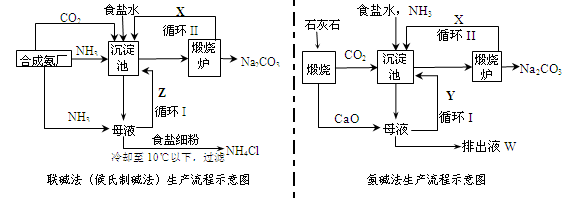
| A£®·Ö±š¼ÓČČX”¢ZµÄ·ŪÄ©£¬½«²śÉśµÄĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®£¬¹Ū²ģĻÖĻó |
| B£®·Ö±š½«X”¢ZÅä³ÉĻ”ČÜŅŗ£¬ÖšµĪµĪ¼ÓĻ”ŃĪĖį£¬¹Ū²ģĻÖĻó |
| C£®·Ö±š½«X”¢ZÅä³ÉĻ”ČÜŅŗ£¬·Ö±š¼ÓČėĀČ»ÆøĘČÜŅŗ£¬¹Ū²ģĻÖĻó |
| D£®·Ö±š½«X”¢ZÅä³ÉĻ”ČÜŅŗ£¬·Ö±š¼ÓČė³ĪĒåŹÆ»ŅĖ®£¬¹Ū²ģĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com