
 一定条件下,在一个3L密闭容器中发生如图反应:
一定条件下,在一个3L密闭容器中发生如图反应:| △c |
| △t |
| ||
| 6min |
| 1 |
| 9 |
| 1 |
| 9 |


科目:高中化学 来源: 题型:
| A、4g重水(D2O)中所含质子数为2NA |
| B、4.48L N2与CO的混合物所含分子数为0.2NA |
| C、12.5mL16 mol?L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| D、某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
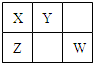 已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )| A、四种元素的原子半径大小rY>rW>rX>rZ |
| B、元素X的含氧酸只有一种,元素Y则有两种 |
| C、元素Z的气态氢化物的稳定性比元素Y的强 |
| D、元素Y和W的氧化物是导致酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| M | ||
| X | Y | Z |
| A、Y的氢化物的沸点一定比M的氢化物的沸点高 |
| B、Z的最高价氧化物对应的水化物有可能是弱电解质 |
| C、这四种元素形成的晶体单质都是分子晶体 |
| D、单质M的晶体中可能含有共价键和分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒容通入惰性气体 |
| B、恒压时通入惰性气体 |
| C、增加CO的浓度 |
| D、加催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了快速配制好溶液,可以用容量瓶直接溶解氯化钠固体来配制溶液 |
| B、Cu中混有CuO,可以通过加入足量盐酸溶液,再过滤、洗涤烘干可得到洁净的Cu |
| C、设NA为阿伏伽德罗常数的值,1.0 L c(H+)=1.0mol/L的硫酸溶液中含有的H+数为NA |
| D、Fe(OH)3胶体是能产生丁达尔效应的分散系,而CuSO4溶液和蒸馏水是不能产生丁达尔效应的分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、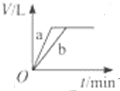 |
C、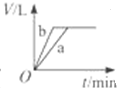 |
D、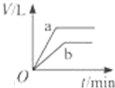 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com