
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前两溶液中H+浓度的大小关系:A=10B | |
| B. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7 mol/L | |
| C. | 取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,所消耗酸溶液的体积相同 | |
| D. | 用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7 |
分析 根据图象可知,室温下,pH相差1的两种一元碱溶液A和B,稀释相同倍数后溶液的pH相等,说明A的pH不会较大,而B的不会较小,则A的碱性大于B,
A.稀释前A溶液中氢氧根离子浓度为B的10倍,则氢离子浓度为B的0.1倍,
B.碱电离出的氢氧根离子抑制了水的电离;
C.M点AB溶液pH相同,而A的碱性大于B,则A的浓度小于B;
D.醋酸是弱酸和一元碱反应生成的盐溶液酸碱性由离子的水解程度决定,恰好反应溶液pH不等于大于7.
解答 解:根据图象可知,室温下,pH相差1的两种一元碱溶液A和B,稀释相同倍数后溶液的pH相等,说明A的pH不会较大,而B的不会较小,则A的碱性大于B,
A.稀释前A溶液的pH比B大1,则A溶液中的氢氧根离子浓度为B的10倍,而A溶液中氢离子浓度应该为B的0.1倍,即:稀释前两溶液中H+浓度的大小关系:10A=B,故A错误;
B.碱溶液抑制了水的电离,则稀释前A溶液中由水电离出的OH-的浓度小于10-7 mol/L,故B错误;
C.M点A、B溶液pH相同,氢氧根离子浓度相同,由于A的碱性大于B,则A的浓度小于B的浓度,加入同浓度的硫酸溶液至恰好完全反应时,A所消耗酸溶液的体积小于B,故C错误;
D.用醋酸中和A溶液至恰好完全反应时,醋酸是弱酸,生成的醋酸根离子水解显碱性,若A为强碱,溶液的pH大于7,若A为弱碱,反应生成弱酸弱碱盐,溶液的pH可能等于或小于7,故D正确;
故选D.
点评 本题考查电解质在水中的电离及图象,题目难度中等,明确图象中pH的变化及交点的意义是解答本题的关键,试题侧重考查学生的分析、理解能力及灵活应用能力.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

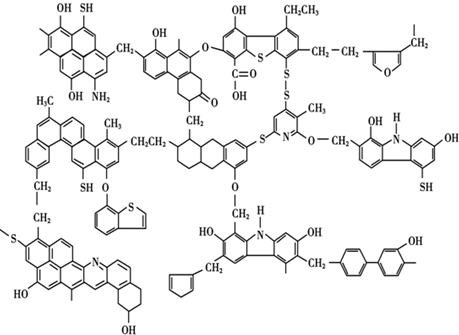
| A. | 与金属钠作用时,键①断 | |
| B. | 燃烧时,①②③④⑤键均断裂 | |
| C. | 和乙酸、浓硫酸共热时,键②断裂 | |
| D. | 在银催化下和氧气反应时,键①和③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | -- | +3 | +4 | +5 | +7 | +1 | +5 | -- |
| 最低价态 | -- | -- | -2 | -- | -4 | -3 | -1 | -- | -3 | -1 |
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应过程中得到6.72 L的气体(标况) | |
| B. | 最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) | |
| C. | 最终得到7.8 g的沉淀 | |
| D. | 最终得到的溶液中c(NaCl)=2.0 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ;CO2的电子式
;CO2的电子式 ;NH4Cl的电子式
;NH4Cl的电子式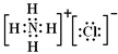 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.
有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为减缓反应速率,将饱和食盐水滴加到烧瓶中的电石上来制取乙炔 | |
| B. | 实验室制乙烯时应将无水乙醇缓慢加入到浓硫酸中,并加入碎瓷片以防暴沸 | |
| C. | 将浓氨水逐滴加入到2%的硝酸银溶液中至产生的沉淀恰好溶解即制得银氨溶液 | |
| D. | 苯甲酸的重结晶实验中,粗苯甲酸全溶后再加入少量蒸馏水,目的是有利于趁热过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a不可能显中性 | B. | a只能显碱性 | C. | b不可能显酸性 | D. | b只能显中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com