
分析 (1)该装置构成原电池,铁发生吸氧腐蚀,将化学能转化为电能;
(2)碳粉作正极,氯化钠溶液为电解质溶液,能使装置构成闭合回路;
(3)负极上铁失电子发生氧化反应,正极上氧气得电子发生还原反应,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被空气氧化生成氢氧化铁,氢氧化铁分解生成氧化铁.
解答 解:(1)该装置符合原电池构成条件,所以能构成原电池,放电时将化学能转化为电能,所以热敷袋放出的热来自于原电池中的氧化还原反应,故答案为:原电池中的氧化还原反应;
(2)炭粉构成原电池正极,正极上氧气得电子发生还原反应,NaCl溶液起电解质溶液作用,从而形成原电池,加速Fe的氧化,
故答案为:炭粉构成原电池正极,NaCl溶液起电解质溶液作用,从而形成原电池,加速Fe的氧化;
(3)负极上铁失电子发生氧化反应,电极反应式为2Fe-4e-═2Fe2+,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4e-═4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,即总反应为:2Fe+O2+2H2O═2Fe(OH)2,氢氧化亚铁不稳定,易被空气氧化生成氢氧化铁,氢氧化铁分解生成氧化铁,反应方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3、2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,故答案为:2Fe-4e-═2Fe2+;2H2O+O2+4e-═4OH-;2Fe+O2+2H2O═2Fe(OH)2、4Fe(OH)2+O2+2H2O═4Fe(OH)3、2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O.
点评 本题考查原电池原理,侧重考查电极反应式的书写等知识点,注意生成铁锈原因,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属铝投入到氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉 Fe3++Fe═2Fe2+ | |
| D. | 二氧化碳通入碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO42-、NO3- | |
| B. | 将过量二氧化硫气体入冷氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 1.0mol•L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO42- | |
| D. | 硫化铜溶于硝酸的离子方程式为CuS+2H+═H2S↑+Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 | |
| B. | 盐酸-混合物 胆矾-纯净物 C60-单质 | |
| C. | 纯碱-碱 硫化氢-酸 小苏打-酸式盐 | |
| D. | 液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱电解质一定是共价化合物 | |
| B. | 氨气溶于水,当c(OH-)=c(NH4+)时,表明NH3•H2O电离处于平衡状态 | |
| C. | 强电解质溶液中不存在溶质分子,弱电解质溶液中存在溶质分子 | |
| D. | 由0.1 mol•L-1一元碱BOH的pH=10,可知溶液中存在BOH═B++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
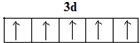 .
.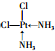 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)═c(CH3COO-)+c(CH3COOH) | |
| B. | 0.1mol•L-1的CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 将CH3COONa溶解到醋酸中,CH3COONa抑制醋酸的电离 | |
| D. | 等物质的量浓度的CH3COONa、CH3COONH4溶液中c(CH3COO-)不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②⑤⑥ | C. | ③④⑤ | D. | ②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com