
����Ŀ����ͼ��ʾ��װ�ã�X��Y���Ƕ��Ե缫������Դ��ͨ���ף��е����̪��Һ����Fe�������Ժ�ɫ��������ʢ��100mL3.00molL��1��CuSO4��Һ���Իش��������⣺ 
��1���ڵ�Դ�У�B�缫Ϊ������缫���ƣ���ͬ������װ���д�ͭΪ����
��2���ڼ�װ���У�ʯī��C���缫�Ϸ�����Ӧ�����������ԭ��������װ�����ܵĻ�ѧ����ʽ�� ��
��3�������װ���о�ͭ�缫������������0.64g�����ʼ�װ���У����缫�ϲ����������ڱ�״����ΪL��
��4���ڱ�װ���У�X�缫�Ϸ����ĵ缫��Ӧʽ�� ��
��5���ڴ˹����У������������缫����������ǡ�����ʱ�����������ҳ��о�ͭ������g��
���𰸡�
��1��������
��2��������2NaCl+2H2O ![]() 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
��3��0.224
��4��2H2O��4e��=4H++O2����4OH����4e��=2H2O+O2��
��5��38.4
���������⣺��1����Ϊ��ⱥ��ʳ��ˮ����Fe�������Ժ�ɫ��˵���ü��������ӷŵ磬������Ũ�ȴ���������Ũ�ȣ���Һ�ʼ��ԣ����Ըõ缫��������C�缫���������������Դ������������A�ǵ�Դ��������B��ԭ��صĸ��������Դ��ǣ���������2���ڼ��У�ʯī�缫Ϊ������������������ʧȥ���ӷ���������Ӧ���������������������ӵõ����ӷ�����ԭ��Ӧ������������Һ��������Ũ���������ɼ����ܷ�ӦʽΪ��2NaCl+2H2O ![]() 2NaOH+H2��+Cl2�������Դ��ǣ�������2NaCl+2H2O
2NaOH+H2��+Cl2�������Դ��ǣ�������2NaCl+2H2O ![]() 2NaOH+H2��+Cl2������3�������װ���о�ͭ�缫������������0.64g���缫��ӦΪ��Cu2++2e��=Cu����ת�Ƶ���Ϊ0.02mol����·�е���ת���غ㣬�������缫�ķ�Ӧ��2H++2e��=H2�������ڱ���²������������Ϊ��0.01mol��22.4L/mol=0.224L�����Դ��ǣ�0.224����4���ڱ�װ���У�XΪ����������������������ʧȥ���ӷ���������Ӧ�����������缫��ӦʽΪ��2H2O��4e��=4H++O2�� ��4OH����4e��=2H2O+O2���� ���Դ��ǣ�2H2O��4e��=4H++O2�� ��4OH����4e��=2H2O+O2������5�������з����ķ�Ӧ�ֱ��ǣ������ϣ�2H2O��4e��=O2��+4H+ �� ������Cu2++2e��=Cu��2H++2e��=H2����100mL3.00molL��1��CuSO4��Һ��ͭ�������ʵ����ǣ�0.3mol��ͭ���ӵõ��ӵ���0.6mol�������缫����������ǡ�����ʱ�������״���£������Ϊnmol����2n+0.6=4n�����n=0.3����װ����ת�Ƶ��ӵ����ʵ�����1.2mol���ҳز�����ͭ�ĵ缫��ӦΪ��Cu2++2e��=Cu����ͭ���أ�
2NaOH+H2��+Cl2������3�������װ���о�ͭ�缫������������0.64g���缫��ӦΪ��Cu2++2e��=Cu����ת�Ƶ���Ϊ0.02mol����·�е���ת���غ㣬�������缫�ķ�Ӧ��2H++2e��=H2�������ڱ���²������������Ϊ��0.01mol��22.4L/mol=0.224L�����Դ��ǣ�0.224����4���ڱ�װ���У�XΪ����������������������ʧȥ���ӷ���������Ӧ�����������缫��ӦʽΪ��2H2O��4e��=4H++O2�� ��4OH����4e��=2H2O+O2���� ���Դ��ǣ�2H2O��4e��=4H++O2�� ��4OH����4e��=2H2O+O2������5�������з����ķ�Ӧ�ֱ��ǣ������ϣ�2H2O��4e��=O2��+4H+ �� ������Cu2++2e��=Cu��2H++2e��=H2����100mL3.00molL��1��CuSO4��Һ��ͭ�������ʵ����ǣ�0.3mol��ͭ���ӵõ��ӵ���0.6mol�������缫����������ǡ�����ʱ�������״���£������Ϊnmol����2n+0.6=4n�����n=0.3����װ����ת�Ƶ��ӵ����ʵ�����1.2mol���ҳز�����ͭ�ĵ缫��ӦΪ��Cu2++2e��=Cu����ͭ���أ� ![]() =38.4g��
=38.4g��
���Դ��ǣ�38.4��


 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.10mol��L��1NH3��H2O��Һ�У���������NH4Cl���������ı仯��
A.NH3��H2O�ĵ���̶ȼ�С
B.NH3��H2O�ĵ��볣������
C.��Һ�ĵ�����������
D.��Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ȷ�Ӧ������������ԭ��Ӧ���ǣ� ��
A.������O2��ȼ�յķ�Ӧ
B.Ba��OH��28H2O��NH4Cl�ķ�Ӧ
C.���ȵ�̼��H2O��g����Ӧ
D.��Ƭ��ϡH2SO4��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��ʵ��ȷ������Ԫ�������ɽ��͵���
��ԭ�Ӱ뾶��Cl��P�ڷе㣺HCl��H2S�ۻ�ԭ�ԣ�S2����C1������ͬ�����µ���̶ȣ�H2CO3��H2SiO3
A. �٢�B. �ۢ�C. ��D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ͬѧ������ʵ��̽��Na2CO3��NaHCO3�����ʣ��ش��������⣺
��1������ͬѧ�ֱ�ȡ1.0g Na2CO3��NaHCO3���壬���μӼ���ˮ������ʢNa2CO3���Թ��¶���������ʢNaHCO3���Թ��¶��½���ԭ���� ��
��2������ͬѧ�ֱ�ȡ0.1mol/L Na2CO3��0.1mol/LNaHCO3����Һ����0.1mol/LHCl��Һ�ζ���pH�仯����������Ĺ�ϵ��ͼ��ʾ�� 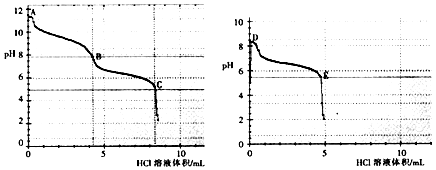
��̼���������ᷴӦpH������ͻ�䣬�ﵽ���η�Ӧ�յ㣬�ֱ�������A��B��C��D��E����
��B�����Ҫ���������û�ѧʽ��ʾ����
��B��������ڡ���С�ڡ��� D���pH����Ҫԭ���� ��
��3������ͬѧԤ��NaHCO3�����ԣ�������Һ����þ�ۣ����������ݺͳ������ɣ�д����ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����µ����Ų�ʽ���ǻ�̬ԭ�ӵĵ����Ų�ʽ���ǣ� ��
A.1s22s1
B.1s22s12p1
C.1s22s22p63s2
D.1s22s22p63s1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�ClO2��2KClO3+H2C2O4+H2SO4 ![]() 2ClO2��+K2SO4+2CO2��+2H2O������˵����ȷ���ǣ� ��
2ClO2��+K2SO4+2CO2��+2H2O������˵����ȷ���ǣ� ��
A.KClO3�ڷ�Ӧ�еõ�����
B.ClO2����������
C.H2C2O4�ڷ�Ӧ�б���ԭ
D.1mol KClO3�μӷ�Ӧ��2 mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. ���ԣ�LiOH>NaOH>KOH>RbOH
B. �����ԣ�Rb>K>Na>Li
C. ���ᷴӦʱFe��ʧ2e-��Naʧe-������Fe�Ľ�����ǿ��Na
D. Rb������ˮ��Ӧ�ų�H2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com