
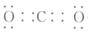
(1)A的化学式是__________________________,
H的电子式是________________________。
(2)反应②的化学方程式是_______________________________。
(3)写出离子方程式:
反应①__________________;反应③_____________________。
(4)在熔融条件下电解Q的化学方程式是_______________________。
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:阅读理解
| 元素 | Al | B | Be | C | Cl | F | Li |
| X | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | Fe |
| X | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | 1.8 |


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A-B | A=B | A≡B | ||||
CO |
键能(KJ/mol) | 357.7 | 798.9 | 1071.9 | ||
| 键能差值(KJ/mol) | 441.2 | 273 | ||||
| N2 | 键能(KJ/mol) | 154.8 | 418.4 | 941.7 | ||
| 键能差值(KJ/mol) | 263.6 | 523.3 | ||||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省太原市高三第一学段测评考试化学试卷 题型:填空题
(12分)如下图所示的转化关系中,已知A是由短周期元素组成的酸式盐。通常状况下,D、E、F、Y、H为气体。G和K均为常见的强酸,D和X的分子中均含有10个电子。请回答下列问题:
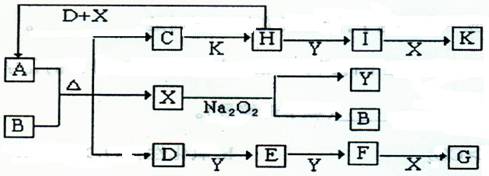
(1)B的电子式为 ,其中含有的化学键类型是 ;C的化学式是 。
(2)写出在加热条件下.A与足量的B溶液反应的离子方程式: 。
(3)写出D与Y在点燃条件下反应,生成X和一种单质的化学方程式: 。
(4)若G的稀溶液溶解了a mol Fe后(假设E是唯一的还原产物),溶液中两种金属阳离子的物质的量恰好相等,则被还原的G是 mol(用含a的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com