
下列溶液中有关物质的量浓度关系正确的是
A.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.0.1 mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3)
C.0.1 mol·L-1NaHCO3溶液与0.2 mol·L-1NaOH溶液等体积混合:c(Na+)>c(OH-)>0.05 mol·L-1>c(CO32-)>c(HCO3-)
D.0.2 mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
以下说法正确的是
A.共价化合物内部可能有极性键和非极性键
B.原子或离子间相互的吸引力叫化学键
C.非金属元素间只能形成共价键
D.金属元素与非金属元素的原子间只形成离子键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)乙基香兰素是一种合成香料,其结构简式如图:
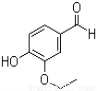
(1)以下推测正确的是 ;
a.从分子结构上看,它属于芳香烃
b.该物质能与FeCl3溶液发生显色反应
c.该物质能与碳酸钠溶液反应产生CO2气体
d.一定条件下,1mol该物质最多能与4molH2发生加成反应
(2)R物质是乙基香兰素的同分异构体,性质如下:
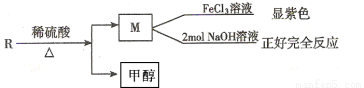
试写出任意一种符合上述条件的R的同分异构体的结构简式 。
(3)X也是乙基香兰素的同分异构体,其可以发生如下反应:
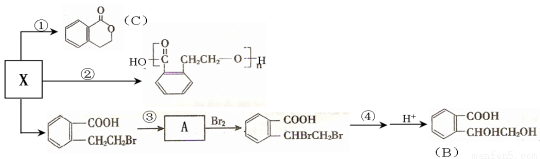
(Ⅰ)X的结构简式 ;B中含氧官能团的名称 ;
(Ⅱ)反应①的反应类型 、化合物C的分子式为 ;
(Ⅲ)反应④的试剂是NaOH的水溶液;反应④的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:选择题
在100mL 0.1 mol·L-1 HA的溶液中,c(H+)=0.05 mol·L-1,往该溶液中加入等体积等浓度的NaOH溶液(忽略溶液混合体积变化),下列离子浓度关系正确的是
A.c(Na+)> c(A-)> c(H+)> c(OH-)
B.c(A-)+ c(HA)=0.05 mol·L-1
C.c(Na+)> c(A-)> c(HA)>c(OH-)
D.c(HA)+ c(H+)= c(A-)+ c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:实验题
(15分)工业上以浓缩海水为原料提取溴的部分流程如下:

已知:Br2常温下呈液态,易挥发,有毒;3Br2+3CO32-===5Br-+BrO3- +3CO2。
(1)上述流程中,步骤①~③的目的是________。
(2)反应釜2中发生反应的离子方程式为____________。
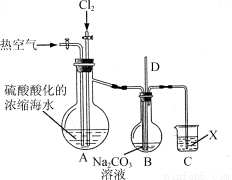
(3)实验室使用右图所示装置模拟上述过程。A装置中先通入Cl2一段时间后,再通入热空气。通入热空气的目的是____________;B装置中导管D的作用是________;C装置中溶液X为________。
(4)对反应后烧瓶B中的溶液进行如下实验,请补充完整相关实验步骤。
限选用的试剂为:稀硫酸、四氯化碳、澄清石灰水。
①检验烧瓶B的溶液中是否含有CO32-。
取烧瓶B中的溶液适量,加入试管中,再加入过量的稀硫酸酸化;____。
②提取反应后烧瓶B溶液中的溴单质。
向烧瓶B中加入过量的稀硫酸酸化;____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高 正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A.X与Y形成的化合物只有一种
B.R的氢化物的热稳定性比W的强
C.原子半径:r(Z)<r(R)
D.Y的最高价氧化物的水化物的酸性比W的强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.中子数为20的氯原子: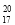 Cl
Cl
B.苯的结构简式:C6H6
C.硅的原子结构示意图: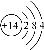
D.Na2S的电子式: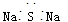
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市高三3月月考化学试卷(解析版) 题型:选择题
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如下表,下列叙述正确的是
酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数 | K a=1.75×10-5 | K a=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
A.25℃,等物质的量浓度的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,碱性最强的是Na2CO3
B.将0.1 mol·L-1的醋酸加水不断稀释,所有离子浓度均减小
C.少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为: SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO- =CO32-+2HClO
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g);ΔH=+49.0 kJ/mol
②CH3OH(g)+ O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ/mol
下列说法正确的是

A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如上图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+ O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol
O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com