

 写出由E转变成F的现象 ;其发生反应的化学方程式________。
写出由E转变成F的现象 ;其发生反应的化学方程式________。 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.X2+具有还原性 | B.X的最高价氧化物具有强氧化性 |
| C.该元素是第ⅥA族元素 | D.X的+2价化合物比+4价化合物稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
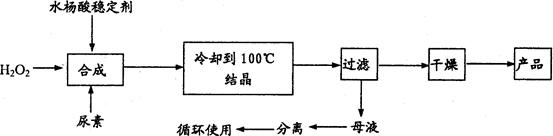
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
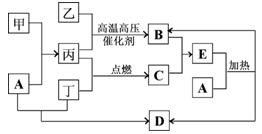
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是
1molF参与反应②时,转移的电子数目为 。反应③中氧化剂与还原剂的物质的量之比为 ,将气体D通人BaCl2溶液中,未见浑浊,如果要使溶液变浑浊,再向溶液中通人的气体可以是  (填2种)。
(填2种)。 ,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。
,反应③的离子方程式是 ;2molG与lmolB化合生成2mol新物质,该物质的分子中所有原子都达到8电子稳定结构,其电子式为 。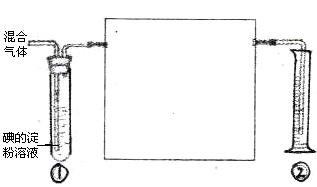
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 离子,加入下列沉淀剂的顺序是(填序号) 。
离子,加入下列沉淀剂的顺序是(填序号) 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
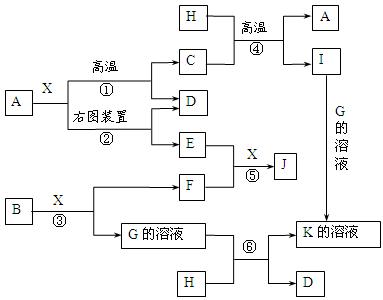
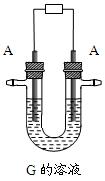
 按要求填空:
按要求填空:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
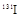 (碘)、
(碘)、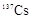 (铯)等。下列说法正确的是( )
(铯)等。下列说法正确的是( )A.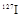 与 与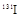 为不同的核素,但具有相同的化学性质 为不同的核素,但具有相同的化学性质 |
B.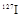 是碘元素稳定的同位素,与 是碘元素稳定的同位素,与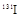 为互为同分异构体 为互为同分异构体 |
C.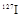 与 与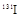 的质量数不同,核外电子排布方式也不同 的质量数不同,核外电子排布方式也不同 |
D.铯为IA元素,常温时,0.1mol·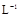 的 的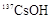 溶液,pH<13 溶液,pH<13 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
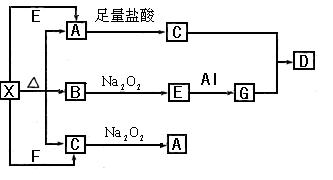
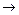 A的离子方程式:_____________________________________
A的离子方程式:_____________________________________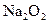 参加反应的化学方程式______________________________________,
参加反应的化学方程式______________________________________,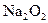 转移的电子数为_____________个。
转移的电子数为_____________个。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com