
��17�֣����л�ԭ�Ե���ˮ��������ɫ�������ᾧ���ɫ��ĩ��������Ũ���Ტ����������������ȥˮ�֣��ֽ�Ϊ������̼��һ����̼��
��1�����ᣨH2C2O4���ֽ�Ļ�ѧ����ʽ Ϊ�� ��
����װ���У������ڲ���ֽ���ȡ������� ��������ĸ��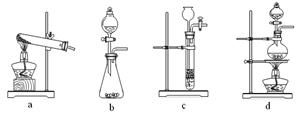
��2��ij̽��С�����ò���ֽ�����Ļ����������ⷴӦ���ⶨ������Ʒ��ɣ��ٶ�������ֻ��Fe2O3��nH2O��Fe���ֳɷݣ���ʵ��װ������ͼ��ʾ����ش�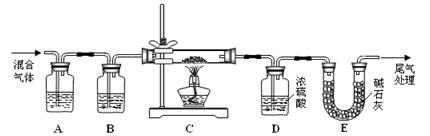
�� Ϊ�� �����������CO���壬ϴ��ƿA��B��ʢ�ŵ��Լ��ֱ��� �� ��
�����������CO���壬ϴ��ƿA��B��ʢ�ŵ��Լ��ֱ��� �� ��
�� �ڵ�ȼ�ƾ���֮ǰӦ���еIJ����ǣ���a�� ����b��ͨ��������һ��ʱ�䡣
�� ȷ������Ʒ������10.00 g����Ӳ�ʲ������У���ַ�Ӧ����ȴ��������Ӳ�ʲ��� ����ʣ���������Ϊ8.32 g��D��Ũ��������0.72 g����n = ���ٶ�Fe��H2O ��������Ӧ��ʵ�������ÿ������ȫ���ջ�Ӧ����
�� �ڱ�ʵ���У����������ʹ�ⶨ���nƫ����� ������ĸ����
a��ȱ��ϴ��ƿB b��ȱ��װ��E
c����Ӧ���������������Fe2O3 d����Ӧ���������������Fe2O3��nH2O
��3����̽��С�黹����KMnO4������Һ��H2C2O4��Һ��Ӧ��������Һ��ɫ��ʧ�ķ������о�Ӱ�췴Ӧ���ʵ����ء�
�� ���������ʵ����Ʊ������в�Ҫ���ո�
��ÿ��ʵ��KMnO4������Һ��������Ϊ4mL��H2C2O4��Һ��������Ϊ2mL������ ��������ѡ��0.5g��0g��
| ʵ�� ��� | ʵ��Ŀ�� | T/K | ��������/g | C/mol��l-1:ѧ����] | |
| KMnO4 | H2C2O4 | ||||
| �� | Ϊ����ʵ�����ο� | 298 | 0.5 | 0.01 | 0.1 |
| �� | ̽��KMnO4������Һ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�� | 298 | 0.5 | 0.001 | 0.1 |
| �� | | 323 | 0.5 | 0.01 | 0.1 |
| �� | ̽�������Է�Ӧ���ʵ�Ӱ�� | | | | 0.1 |
��17�֣� ����
��Ŀ�����л�ѧ
��Դ��
���ͣ��Ķ�����
��Ŀ�����л�ѧ
��Դ��
���ͣ��Ķ�����
��Ŀ�����л�ѧ
��Դ��
���ͣ��Ķ�����
��17�֣����л�ԭ�Ե���ˮ��������ɫ�������ᾧ���ɫ��ĩ��������Ũ���Ტ����������������ȥˮ�֣��ֽ�Ϊ������̼��һ����̼�� ��1�� ���ᣨH2C2O4���ֽ�Ļ�ѧ����ʽ Ϊ�� �� ����װ���У������ڲ���ֽ���ȡ������� ��������ĸ�� ��2�� ij̽��С�����ò���ֽ�����Ļ����������ⷴӦ���ⶨ������Ʒ��ɣ��ٶ�������ֻ��Fe2O3��nH2O��Fe���ֳɷݣ���ʵ��װ������ͼ��ʾ����ش� �� Ϊ�õ����������CO���壬ϴ��ƿA��B��ʢ�ŵ��Լ��ֱ��� �� �� �� �ڵ�ȼ�ƾ���֮ǰӦ���еIJ����ǣ���a�� ����b��ͨ��������һ��ʱ�䡣 �� ȷ������Ʒ������10.00 g����Ӳ�ʲ������У���ַ�Ӧ����ȴ��������Ӳ�ʲ��� ����ʣ���������Ϊ8.32 g��D��Ũ��������0.72 g����n= ���ٶ�Fe��H2O ��������Ӧ��ʵ�������ÿ������ȫ���ջ�Ӧ���� �� �ڱ�ʵ���У����������ʹ�ⶨ���nƫ����� ������ĸ���� a��ȱ��ϴ��ƿB b��ȱ��װ��E c����Ӧ���������������Fe2O3 d����Ӧ���������������Fe2O3��nH2O ��3�� ��̽��С�黹����KMnO4������Һ��H2C2O4��Һ��Ӧ��������Һ��ɫ��ʧ�ķ������о�Ӱ�췴Ӧ���ʵ����ء� �� ���������ʵ����Ʊ������в�Ҫ���ո� ��ÿ��ʵ��KMnO4������Һ��������Ϊ4mL��H2C2O4��Һ��������Ϊ2mL������ ��������ѡ��0.5g��0g�� ʵ�� ��� ʵ��Ŀ�� T/K ��������/g C/mol��l-1:] KMnO4 H2C2O4 �� Ϊ����ʵ�����ο� 298 0.5 0.01 0.1 �� ̽��KMnO4������Һ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�� 298 0.5 0.001 0.1 �� 323 0.5 0.01 0.1 �� ̽�������Է�Ӧ���ʵ�Ӱ�� 0.1 �� ��Ҫȷ���㷴Ӧ���ʣ���ʵ���л���ⶨ��Һ��ɫ��ʧ����Ҫ��ʱ�䡣������Ƴ� ͨ���ⶨ��ɫʱ�䳤�����ж�Ũ�ȴ�С�뷴Ӧ���ʹ�ϵ��ʵ�鷽�� ��
��Ŀ�����л�ѧ
��Դ��2010-2011ѧ�긣��ʡ��ƽ�б�ҵ����Ӧ�Կ��ԣ����ۣ���ѧ����
���ͣ�ʵ����
��17�֣����л�ԭ�Ե���ˮ��������ɫ�������ᾧ���ɫ��ĩ��������Ũ���Ტ����������������ȥˮ�֣��ֽ�Ϊ������̼��һ����̼�� ��1�� ���ᣨH2C2O4���ֽ�Ļ�ѧ����ʽ Ϊ��
��
����װ���У������ڲ���ֽ���ȡ�������
��������ĸ�� ��2�� ij̽��С�����ò���ֽ�����Ļ����������ⷴӦ���ⶨ������Ʒ��ɣ��ٶ�������ֻ��Fe2O3��nH2O��Fe���ֳɷݣ���ʵ��װ������ͼ��ʾ����ش� �� Ϊ�õ����������CO���壬ϴ��ƿA��B��ʢ�ŵ��Լ��ֱ��� ��
�� �� �ڵ�ȼ�ƾ���֮ǰӦ���еIJ����ǣ���a�� ����b��ͨ��������һ��ʱ�䡣 �� ȷ������Ʒ������10.00 g����Ӳ�ʲ������У���ַ�Ӧ����ȴ��������Ӳ�ʲ��� ����ʣ���������Ϊ8.32 g��D��Ũ��������0.72 g����n
=
���ٶ�Fe��H2O ��������Ӧ��ʵ�������ÿ������ȫ���ջ�Ӧ���� �� �ڱ�ʵ���У����������ʹ�ⶨ���nƫ�����
������ĸ����
a��ȱ��ϴ��ƿB
b��ȱ��װ��E c����Ӧ���������������Fe2O3 d����Ӧ���������������Fe2O3��nH2O ��3�� ��̽��С�黹����KMnO4������Һ��H2C2O4��Һ��Ӧ��������Һ��ɫ��ʧ�ķ������о�Ӱ�췴Ӧ���ʵ����ء� �� ���������ʵ����Ʊ������в�Ҫ���ո� ��ÿ��ʵ��KMnO4������Һ��������Ϊ4mL��H2C2O4��Һ��������Ϊ2mL������ ��������ѡ��0.5g��0g�� ʵ�� ��� ʵ��Ŀ�� T/K ��������/g C/mol��l-1:] KMnO4 H2C2O4 �� Ϊ����ʵ�����ο� 298 0.5 0.01 0.1 �� ̽��KMnO4������Һ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�� 298 0.5 0.001 0.1 �� 323 0.5 0.01 0.1 �� ̽�������Է�Ӧ���ʵ�Ӱ�� 0.1 �� ��Ҫȷ���㷴Ӧ���ʣ���ʵ���л���ⶨ��Һ��ɫ��ʧ����Ҫ��ʱ�䡣������Ƴ� ͨ���ⶨ��ɫʱ�䳤�����ж�Ũ�ȴ�С�뷴Ӧ���ʹ�ϵ��ʵ�鷽��
��
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
��1�� H2C2O4 CO�� + CO2�� +
CO�� + CO2�� +  H2O ��2�֣� d ��2�֣�
H2O ��2�֣� d ��2�֣�
��2����ŨNaOH��Һ��1�֣� Ũ���ᣨ1�֣�
�ڼ��װ�������ԣ������ž�װ���ڿ������Է�ֹ����ʱ������ը�� ��1�֣�
��2��2�֣� �� a b c��2�֣�
��3����4�֣���ʵ��
���ʵ��Ŀ�� T/K ������
����/gC/(mol/L) KMnO4 H2C2O4 �� �� �� ̽���¶ȶԷ�Ӧ���ʵ�Ӱ�� �� 298 

�¿γ�ѧϰ��Դѧϰ�ֲ�ϵ�д�
�������ϵ�д�
��Կ��Сѧ��ҵ�ܸ�ϰϵ�д�
��Ԫ�¿���ϵ�д�
С����ϵͳ�ܸ�ϰָ������ϵ�д�
������������ϵ�д�
Сѧ��ҵ��ѧ��ϰ������18���Ծ�ϵ�д�
С�۶��Ķ������ĸ�Чѵ��ϵ�д�
�ܸ�ϰϵͳǿ��ѵ��ϵ�д�
С������ϵ�д�

�꼶
���пγ�
�꼶
���пγ�
��һ
��һ��ѿγ��Ƽ���
��һ
��һ��ѿγ��Ƽ���
�߶�
�߶���ѿγ��Ƽ���
����
������ѿγ��Ƽ���
����
������ѿγ��Ƽ���
����
������ѿγ��Ƽ���
��1�����ᣨH2C2O4���ֽ�Ļ�ѧ����ʽΪ��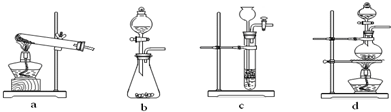
��2��ij̽��С�����ò���ֽ�����Ļ����������ⷴӦ���ⶨ������Ʒ��ɣ��ٶ�������ֻ��Fe2O3?nH2O
��Fe���ֳɷݣ���ʵ��װ������ͼ��ʾ����ش�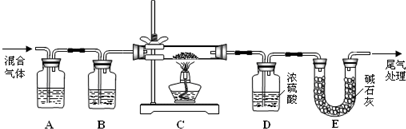
��Ϊ�õ����������CO���壬ϴ��ƿA��B��ʢ�ŵ��Լ��ֱ���
���ڵ�ȼ�ƾ���֮ǰӦ���еIJ����ǣ���a��
��ȷ������Ʒ������10.00g����Ӳ�ʲ������У���ַ�Ӧ����ȴ��������Ӳ�ʲ�������ʣ���������Ϊ8.32g��D��Ũ��������0.72g����n=
���ڱ�ʵ���У����������ʹ�ⶨ���nƫ�����
a��ȱ��ϴ��ƿB b��ȱ��װ��E
c����Ӧ���������������Fe2O3 d����Ӧ���������������Fe2O3?nH2O
��3����̽��С�黹����KMnO4������Һ��H2C2O4��Һ��Ӧ��������Һ��ɫ��ʧ�ķ������о�Ӱ�췴Ӧ���ʵ����أ�
�����������ʵ����Ʊ������в�Ҫ���ո�
��ÿ��ʵ��KMnO4������Һ��������Ϊ4mL��H2C2O4��Һ��������Ϊ2mL������
��������ѡ��0.5g��0g��
ʵ��
���ʵ��Ŀ��
T/K
��������/g
C/mol?l-1
KMnO4
H2C2O4
��
Ϊ����ʵ�����ο�
298
0.5
0.01
0.1
��
̽��KMnO4������Һ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ��
298
0.5
0.001
0.1
��
323
0.5
0.01
0.1
��
̽�������Է�Ӧ���ʵ�Ӱ��
0.1
����Ҫȷ���㷴Ӧ���ʣ���ʵ���л���ⶨ��Һ��ɫ��ʧ����Ҫ��ʱ�䣮������Ƴ�ͨ���ⶨ��ɫʱ�䳤�����ж�Ũ�ȴ�С�뷴Ӧ���ʹ�ϵ��ʵ�鷽��
���о����⡿̽���Ҷ����ijЩ����
���������ϡ��Ҷ��ᣨHOOC-COOH���׳Ʋ��ᣬ����Ҫ�����������£�
��֪��
����
�Ҷ���
�Ҷ��ᾧ��
����ʽ
H2C2O4
H2C2O4?2H2O
��ɫ״̬
��ɫ����
��ɫ����
�ܽ�ȣ�g��
8.6��20�棩
-
�۵㣨�棩
189.5
101.5
�ܶȣ�g?cm-3��
1.900
1.650
�ٲ�����100��ʱ��ʼ������157��ʱ��������������ʼ�ֽ⣮
�ڲ���Ʋ�����ˮ��
�۲���������ʹ����ʯ��ˮ����ǣ�
�ܲ��������ڵ����¿�����Ϊ���壮
�������������ṩ����Ϣ���ش��������⣺
��������롿
������һ�����ݲ��ᾧ�����ɶ���ֽ������в���
��Ʒ�����
��1����С��ͬѧ���������ΪCO��CO2��H2O����������װ�����һ��̽��ʵ��װ�ã����ᾧ��ֽ�װ���ԣ�װ�ÿ��ظ�ʹ�ã����ӵ�����ȥ����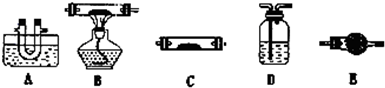
A��ˮ��װ��ˮ����B��װ����ͭ��C��װ��ˮ����ͭ��D��װ����ʯ��ˮ��E��װ��ʯ��
��ش��������⣺
��װ�õ�����˳��Ϊ��A��
�ڼ��������CO��ʵ��������
������װ���Ƿ���ڲ�����֮����
����������Ҷ������������
��Ʒ�����
��2����С��ͬѧΪ��֤����������������������ʵ�飬�����ܴﵽʵ��Ŀ����
A�������ᾧ�����ں���̪��NaOH��Һ�У���Һ��ɫ
B���ⶨ��ͬŨ�ȵIJ����������Һ��pH
C���ⶨ�����ƣ�Na2C2O4����Һ��pH
D����������Һ����Na2CO3��Һ�У���CO2�ų�
�����������Ҷ�����л�ԭ��
��Ʒ�����
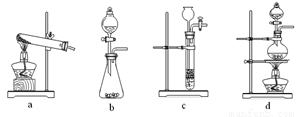
��3����С��ͬѧ���������ữ��KMnO4��Һ�е�������IJ�����Һ����������KMnO4��Һ��ɫ���Ӷ��жϲ�����н�ǿ�Ļ�ԭ�ԣ���ƽ�÷�Ӧ�����ӷ���ʽ��
��4����������ԭ���ɶ����ⶨij���ᾧ����Ʒ������H2C2O4?2H2O������һЩ���ʣ���H2C2O4?2H2O�ĺ�����
�����ǣ���ȡ����Ʒ0.12g��������ˮ��ȫ�ܽ⣬Ȼ����0.020mol?L-1������KMnO4��Һ�ζ����յ㣨���ʲ����뷴Ӧ�����ζ�ǰ��ζ����е�Һ�������ͼ��ʾ����λ��mL������ò��ᾧ����Ʒ��H2C2O4?2H2O����������Ϊ
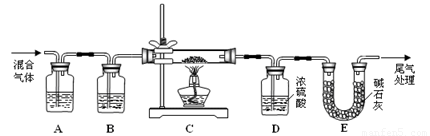
��Ȩ��������վ�������£�ͼƬ��Դ�����磬����Ȩ����Ȩ��ԭ�������У�ת�������ַ���Ȩ��������Ȩ����������������֪�����ǽ����촦������ϵqq��3310059649��
ICP�������: ��ICP��07509807��-10 ����������42018502000812��