
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水;
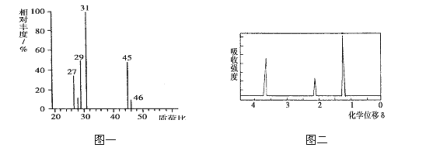
②用质谱仪检测有机物 M,得到如图一所示的质谱图;
③用核磁共振仪处理有机物 M,得到如图二所示图谱,图中三个峰面积之比为1:2:3
试回答下列问题:
⑴M 的结构简式是______________。
⑵N 中含有的官能团的结构简式为_________________________。
【答案】CH3CH2OH —COOH
【解析】
(1)根据质荷比可以知道,有机物M的相对分子质量;根据n=![]() 计算生成的水的物质的量,计算碳元素、氢元素的质量,根据质量守恒判断有机物M是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物M中C、H、O原子个数比值确定最简式,再由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,结合有机物的分子式确定其可能的结构;
计算生成的水的物质的量,计算碳元素、氢元素的质量,根据质量守恒判断有机物M是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物M中C、H、O原子个数比值确定最简式,再由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,结合有机物的分子式确定其可能的结构;
(2)由M 能被酸性高锰酸钾氧化生成 N推出N的结构,写出其官能团的结构简式。
(1)在M的质谱图中,最大质荷比为46,所以其相对分子质量也是46。
将4.6 g该有机物完全燃烧,生成0.2mol CO2和5.4g水,即0.1mol该有机物,含碳:n(C)=n(CO2)=0.2mol,含有的碳原子的质量为m(C)=0.2 mol×12 gmol-1=2.4g,氢原子的物质的量为:n(H)=![]() ×2=0.6 mol,氢原子的质量为m(H)=0.6 mol×1 gmol-1=0.6g,该有机物中m(O)=4.6 g-2.4 g-0.6 g=1.6 g,氧元素的物质的量为n(O)=
×2=0.6 mol,氢原子的质量为m(H)=0.6 mol×1 gmol-1=0.6g,该有机物中m(O)=4.6 g-2.4 g-0.6 g=1.6 g,氧元素的物质的量为n(O)=![]() =0.1mol,则n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.6 mol:0.1 mol=1:2:6:1,所以M分子式为:C2H6O。
=0.1mol,则n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.6 mol:0.1 mol=1:2:6:1,所以M分子式为:C2H6O。
由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,故该有机物结构式为CH3CH2OH,
因此,本题正确答案是:CH3CH2OH;
(2)根据以上分析,M为乙醇,由M 能被酸性高锰酸钾氧化生成 N可知,N为乙酸CH3COOH,N 中含有的官能团的结构简式为—COOH,
因此,本题正确答案是:—COOH。


科目:高中化学 来源: 题型:
【题目】NaNO2一种食品添加剂,它致癌。酸性KMnO4溶液与NaNO2的反应方程式是MnO4-+NO2-+![]() →Mn2++NO3-+H2O。下列叙述中正确的是( )
→Mn2++NO3-+H2O。下列叙述中正确的是( )
A.该反应中NO2-被还原
B.反应过程中溶液的pH减小
C.生成1molNaNO3需消耗0.4 mol KMnO4
D.![]() 中的粒子是OH-
中的粒子是OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,醋酸溶液中存在电离平衡:CH3COOH ![]() CH3COO- + H+
CH3COO- + H+
(1)某温度时,0.1 mol·L-1的醋酸溶液中的c(H+) 与0.01 mol·L-1 的醋酸溶液中的c(H+)的比值 ____(填“大于”“小于”或“等于”)10,理由是_________。
(2)常温下0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是:_____________。
A.c(H+) B.![]() C.c(H+)·c(OH) D.c(OH)/c(H+)
C.c(H+)·c(OH) D.c(OH)/c(H+)
(3)现有pH均为3的醋酸、硫酸两瓶溶液:
①设两种溶液的物质的量浓度依次为c1、c2,则其关系式为_________(用“<”“>”或“=”表示,下同)。
②取相同体积的两种酸分别加入等体积的蒸馏水后,再分别加入少量等量的锌粉,反应开始时放出氢气的速率依次为v1、v2,则其关系式为_______,反应结束放出的氢气的体积依次为V1、V2,则其关系式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述不正确的是( )
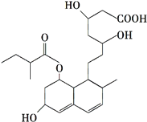
A. 3个—OH皆可因催化氧化生成醛基
B. 能使酸性KMnO4溶液褪色
C. 能发生加成、取代、消去反应
D. 1 mol该物质最多可与2mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.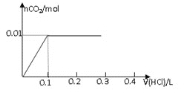
B.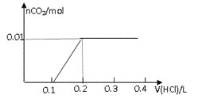
C.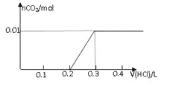
D.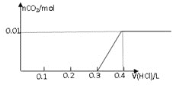
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 按系统命名法,![]() 的名称为2,4,5-三甲基己烷
的名称为2,4,5-三甲基己烷
B. 3-甲基-3-乙基戊烷的一氯取代产物有6种
C. 化合物![]() 是苯的同系物
是苯的同系物
D. 分子![]() 中,位于同一平面上碳原子最多有6个
中,位于同一平面上碳原子最多有6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、氯、氮是三种常见的非金属元素。
完成下列填空:
(1)我们祖先的四大发明之一黑火药的爆炸反应为:S+2KNO3+3C A+N2↑+3CO2↑(已配平)。氮原子核外电子排布式为______________,生成物固体 A属于_____晶体。
(2)工业合成氨可以实现大规模固氮,氨可用于生产氯化铵、硫酸铵等化学肥料,等物质的量浓度的两溶液相同温度下pH大小为:氯化铵___________硫酸铵(选填>、=或<)。
(3)工业上在催化剂条件下,用NH3作为还原剂将烟气中的NO2还原成无害的氮气和水,反应方程式可表示为:8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目______,若该反应氧化产物比还原产物多0.1mol,被吸收的NO2在标准状况下的体积为_________。
7N2(g)+12H2O(g),用单线桥标出该反应电子转移的方向和数目______,若该反应氧化产物比还原产物多0.1mol,被吸收的NO2在标准状况下的体积为_________。
(4)氯水成分的多样性决定了其性质的复杂性,氯气可用作自来水生产过程中的消毒剂,写出其中主要的化学反应方程式______________________________,在硝酸银溶液中滴加氯水,可以看到有白色沉淀产生,起作用的微粒是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答问题。
(1)Si的基态原子核外电子排布式____,S的基态原子核外有____个未成对电子
(2)用“<”“>”填空
离子半径 | 电负性 | 熔点 | 酸性 |
O2-____Na+ | N___O | 金刚石_____晶体硅 | 硫酸___高氯酸 |
(3)第三周期某元素的电离能情况如图所示,则该元素位于元素周期表第____列
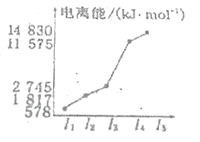
(4)Mn、Fe均为第4周期的过渡元素,两元素的部分电离能数据列于下表:
元素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,对此,你的解释是______。
(5)下图能表示HF分子形成的是(____)
a.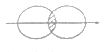 b.
b.![]()
c.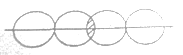 d.
d.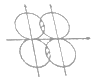
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于____(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是____(填字母)。
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a.石灰石 b.粗盐 c.纯碱
(2)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为____、糖类和蛋白质。淀粉在人体内水解的最终产物是____。
②维生素是人体需要的营养物质。如图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是____,甜味剂是___。泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和___反应释放出了气体。

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。
①控制燃煤产生的SO2排放,能够减少____型酸雨的形成。燃煤排放的烟气中还含有其他污染物,请列举一种:_____。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式_____。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是_____。
③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com