
| A. | 金属氧化物 氧化铁 FeO | B. | 酸性氧化物 二氧化硫 SO2 | ||
| C. | 酸 硫酸 H2SO4 | D. | 碱 纯碱 Na2CO3 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
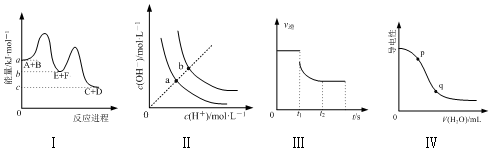
| A. | 图Ⅰ表示反应A+B═C+D的△H=(a-c) kJ•mol-1 | |
| B. | 图Ⅱ表示不同温度下水溶液中H+和OH-的浓度变化曲线,图中a点对应温度高于b点 | |
| C. | 图Ⅲ表示N2+3H2?2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强 | |
| D. | 图Ⅳ表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点pH大于q点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入FeCl3浓溶液或固体后,溶液颜色加深 | |
| B. | 加入少量KCl固体,增大了生成物浓度,平衡向逆反应方向移动,溶液颜色变浅 | |
| C. | 滴加几滴NaOH溶液,有红褐色沉淀生成,溶液颜色加深 | |
| D. | 加入几滴AgNO3溶液,有白色沉淀生成,溶液颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业合成氨生产中增大压强 | |
| B. | 在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 | |
| C. | NO2气体加压后颜色先变深再变浅 | |
| D. | 工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6g 12C中约含有3.01×1023个碳原子 | |
| B. | 1 mol任何物质都含有6.02×1023个分子 | |
| C. | 1 mol O2的质量是32 g•mol-1 | |
| D. | 64 g氧相当于2 mol氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-是该反应的催化剂,它可增加该反应的活化分子百分数 | |
| B. | H2O2分解的反应快慢主要由反应①决定的 | |
| C. | 反应速率与I-的浓度有关 | |
| D. | 2v(H2O2)=2v(H2O)=v(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标态下 22.4 升氧气 | |
| B. | 常温常压下 66 克的 CO2 | |
| C. | 1.2mol 的硫酸 | |
| D. | 100ml,0.1mol•L-1 的氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
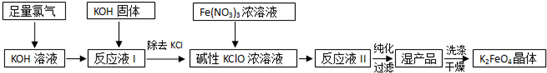
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com