
| A. | 需要加热的反应一定是吸热反应 | |
| B. | 反应是放热还是吸热需要看反应物和生产物所具有的总能量的相对大小 | |
| C. | 放热反应在常温下一定很容易发生 | |
| D. | 化学反应都伴随能量变化,而且都表现为热量变化 |
分析 A.某些放热反应也需要加热才能发生,吸热反应不需要加热也可以发生反应;
B.生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反;
C.放热反应在常温下不一定很容易发生,吸热反应在常温下不一定不能发生;
D.化学反应的能量变化可以是热能、光能、电能等.
解答 解:A.某些放热反应也需要加热才能发生,如铝热剂发生的反应是放热反应,需要加热发生反应,吸热反应不需要加热也可以发生反应,如氢氧化钡晶体和氯化铵的反应为吸热反应,常温下能发生反应,故A错误;
B.生成物的总能量低于反应物总能量的反应,是放热反应,若是吸热反应则相反,所以反应是放热还是吸热取决于反应物和生成物的总能量的相对大小,故B正确;
C.放热反应在常温下不一定很容易发生,如碳与氧气的反应为放热反应,但须点燃,故C错误;
D.化学反应的能量变化可以是热能、光能、电能等等,不仅仅是热能,故D错误;
故选B.
点评 本题考查了化学反应中能量变化的形式、焓变与反应条件无关,注意基础知识的积累,题目难度不大.


科目:高中化学 来源: 题型:解答题
 化石燃料的燃烧会产生大量污染大气的二氧化硫和温室气体二氧化碳,而氢气被认为是无碳无污染的清洁能源.
化石燃料的燃烧会产生大量污染大气的二氧化硫和温室气体二氧化碳,而氢气被认为是无碳无污染的清洁能源.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
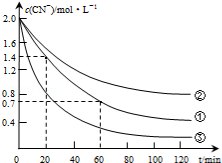 生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).
生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | 双氧水的浓度对破氰反应速率的影响 | 7 | 60 | 10 | 20 | 10 |
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
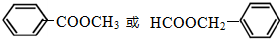 (任写一种).
(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含11个质子、12个中子、10个电子的粒子 | |
| B. | 含18个质子、22个中子、18个电子的粒子 | |
| C. | 含17个质子、18个中子、17个电子的粒子 | |
| D. | 含17个质子、20个中子、18个电子的粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的氧化剂为N2,还原产物为CO | |
| B. | 反应中每生成0.1mol Si3N4转移电子的物质的量为1.2mol | |
| C. | 增大压强平衡向正反应方向移动 | |
| D. | 反应平衡常数表示为K=$\frac{c(CO)}{c({N}_{2})}$,升高温度K值增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体 | |
| B. | 除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去氧化铝中混有的少量二氧化硅,用足量的稀盐酸溶解后过滤 | |
| D. | 除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
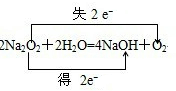
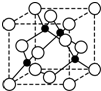 A、B、C、D、E、F是周期表前四周期的元素,且原子序数依次递增,已知A是宇宙中含量最多的元素,B元素能形成的化合物种类最多,E原子的半径是所在周期最大的,E和D形成的某化合物是呼吸面具中气的来源,F基态原子有6个来成对电子.请回答下列问题:
A、B、C、D、E、F是周期表前四周期的元素,且原子序数依次递增,已知A是宇宙中含量最多的元素,B元素能形成的化合物种类最多,E原子的半径是所在周期最大的,E和D形成的某化合物是呼吸面具中气的来源,F基态原子有6个来成对电子.请回答下列问题: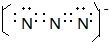 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH=CH2和CH2=CH2的最简式相同 | |
| B. | 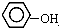 与 与 互为同系物 互为同系物 | |
| C. | 下列物质的沸点按由低到高顺序为:(CH3)2CHCH3<(CH3)4C<(CH3)2CHCH2CH3<CH3(CH2)3CH3 | |
| D. | 等质量的甲烷、乙醇、乙醛分别充分燃烧,所耗用氧气的量依次减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com