
镁与稀硝酸的反应为:Mg+ HNO3(稀)—— Mg(NO3)2+ NH4NO3+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。
(2)该反应中,还原产物是_________,HNO3表现了________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为________。
(1) ;(2)NH4NO3;氧化性,酸性;(3)0.125 mol
;(2)NH4NO3;氧化性,酸性;(3)0.125 mol
【解析】
试题分析:(1)Mg+ HNO3(稀)—— Mg(NO3)2+ NH4NO3+ H2O,Mg由0价变成了+2价化合价↑2,N由+5价变成了-3价↓8,最小公倍数是8,Mg系数×4,Mg(NO3)2系数×4,通过观察反应前后N守恒,HNO3系数×10,最后H守恒,H2O×3,得出:4Mg+10HNO3(稀)=== 4 Mg(NO3)2+NH4NO3+3H2O;(2)N的化合价降低被还原,同时反应后NO3-的存在,因此NH4NO3是还原产物,HNO3既表现氧化性,又表现酸性;(3)HNO3→NH4NO3,生成1molNH4NO3时,共转移8mole-,现在转移了6.02×1023个电子,则被还原的硝酸的物质的量 mol=0.125mol。
mol=0.125mol。
考点:考查氧化还原反应电子转移的表示方法、化学方程式的配平及计算。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年广东省揭阳市高三学业水平考试理综化学试卷(解析版) 题型:填空题
(15分)酯类化合物在医药和涂料等应用广泛。
(1)某有机物X的结构简式如图所示,则下列有关说法正确的是(双选)

A.X在一定条件下能发生加成反应、加聚反应和取代反应
B.在Ni催化下,1 mol X最多只能与1 mol H2加成
C.可用酸性高锰酸钾溶液区分苯和X
D.X核磁共振氢谱有10个吸收峰
(2)固定CO2能有效利用资源、减缓温室效应并制备某些酯类。某高分子F可用下列途径制得:
化合物B分子式为 ,1mol化合物B完全燃烧需要消耗 mol O2 。
(3)化合物A可由芳香族化合物Ⅰ或Ⅱ通过消去反应获得,但只有Ⅰ能与Na反应产生H2,则化合物Ⅰ的结构简式为 (任写一种);由化合物Ⅱ生成A的反应条件为 。
(4)写出由D与足量NaOH溶液反应生成E的化学反应方程式: 。
(5)化合物Ⅲ的结构简式为 在一定条件下,化合物Ⅲ也能与CO2发生类似于化合物C与CO2反应生成D的反应,生成两种化合物(互为同分异构体),写出其中任意一种化合物的结构简式: 。
在一定条件下,化合物Ⅲ也能与CO2发生类似于化合物C与CO2反应生成D的反应,生成两种化合物(互为同分异构体),写出其中任意一种化合物的结构简式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015天津市和平区高一上学期期末考试化学试卷(解析版) 题型:实验题
根据要求完成下列各题实验目的.(a、b为弹簧夹,加热及固定装置已略去)
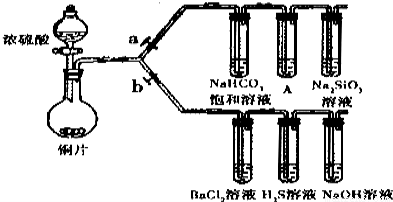
(1)验证碳、硅非金属性的相对强弱.
①实验操作:连接仪器、______、加入药品,打开a关闭b,滴入浓硫酸,加热.
②铜与浓硫酸反应发生的化学方程式是______.
③能说明碳的非金属性比硅强的实验现象是:______.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①打开b,关闭a.能验证SO2具有氧化性的化学方程式是______.
②若大量二氧化硫通入氢氧化钠溶液中,化学方程式________________________
③BaCl2溶液中无沉淀现象,将其分成两份,分别低价下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 |
查看答案和解析>>
科目:高中化学 来源:2014-2015天津市和平区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于浓硫酸,浓硝酸的叙述正确的是
A.加热条件下,均能与碳反应 B.长期露置在空气中,浓度均会升高
C.常温下均不能用铁质容器贮存 D.常温下均能与铜片迅速反应
查看答案和解析>>
科目:高中化学 来源:2014-2015天津市和平区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于物质应用的说法,错误的是
A.玻璃容器可长期盛放各种酸 B.纯碱可以清洗油污
C.浓氨水可检验氯气管道漏气 D.自来水通入少量氯气进行消毒
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:选择题
下列做法正确的是
A.厨房天然气泄漏时,立即开灯查找泄漏处
B.为了增强洁厕液的效果,向其中加入适量漂粉精
C.少量浓硫酸沾在皮肤上,立即涂擦氢氧化钠溶液
D.泡温泉时发生H2S中毒,迅速将患者转移到空气新鲜处
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:选择题
现有三组混合物:①汽油和氯化钠溶液 ②碘的CCl4溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.萃取、蒸发、分液 B.分液、蒸馏、萃取
C.分液、萃取、蒸馏 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三上学期第五次月考理综化学试卷(解析版) 题型:填空题
27.(14分)氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用。试回答下列问题:
(1)N2和H2为原料合成氨气的反应为:N2(g)+3H2(g) 2NH3(g) △H<0,下列措施可以提高H2的转化率是(填选项序号) 。
2NH3(g) △H<0,下列措施可以提高H2的转化率是(填选项序号) 。
a.选择适当的催化剂 b.增大压强
c.及时分离生成的NH3 d.升高温度
(2)在恒温条件下,将N2与H2按一定比例混合的气体充入一个2L固定容积的密闭容器中,10分钟后反应达平衡时,n(N2)=1.0mol,n(H2)=1.0mol,n(NH3)=0.4mol,则反应速率v(N2)= mol/(L·min)。
(3)在容积恒定的密闭容器中进行反应2NO(g)+O2(g) 2NO2(g) △H>0
2NO2(g) △H>0
该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) 。

a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施一定是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t0-t5时,容器内NO2的体积分数在t3-t4时值的最大
(4)氨和联氨(N2H4)是氮的两种常见化合物,最常见的制备联氨的方法是以丙酮为催化剂,用次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式: 。
(5)已知:N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol
若有17 g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为 。
(6)直接供氨式碱性燃料电池的电池反应式是4NH3 + 3O2 = 2N2 + 6H2O,电解质溶液一般使用KOH溶液,则负极电极反应式是 .从理论上分析,该电池工作过程中 (填“需要”或“不需要”)补充碱(KOH).
查看答案和解析>>
科目:高中化学 来源:2015-2015湖南省高二12月学科联赛化学试卷(解析版) 题型:选择题
11.已知温度T时水的离子积常数为 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,
D.混合溶液中,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com