
分析 (1)有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;
(2)相同元素组成,不同形态的单质互为同素异形体;
(3)氢与氧能构成三原子的化合物为水,选取O质量最大的和T构成即可;
(4)氧元素的近似相对原子量为各原子的相对原子量与其百分含量之积的和.
解答 解:①168O、178O、188O 质子数相同,中子数不同,互为同位素;
②H2O、D2O都是水分子;
③石墨、金刚石是由碳元素形成的不同单质,互为同素异形体;
④H、D、T是质子数相同,中子数不同,互为同位素;
(1)互为同位素的是:①,④;
(2)互为同素异形体的是③;
(3)氢与氧能构成三原子的化合物为水,相对分子质量最大的就是两种原子质量数最大的原子构成的,即${{T}_{2}}_{8}^{18}O$;
(4)17O、18O在自然界中所占的原子个数百分比分别为:0.037%和0.204%,则168O的个数百分比为100%-0.037%-0.204%=99.759%,氧元素的近似相对原子质量为:(16×99.759%+17×0.037%+18×0.204%)=16,故答案为:①④;③;${{T}_{2}}_{8}^{18}O$;16.
点评 本题考查同位素、同素异形体的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同种物质等概念的区别是考试的热点问题.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为566.0 kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3 kJ | |
| D. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1453.28 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
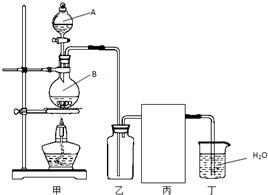 (1)实验室制备HCl气体的反应为:
(1)实验室制备HCl气体的反应为:| 实验 次数 | 草酸溶液的体积 (mL) | ||
| 1 | 20.00 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3(固) | B. | NaCl溶液 | C. | KNO3溶液 | D. | CuSO4(固) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
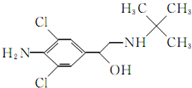 食品安全是现今百姓生活中热议问题之一,瘦肉精学名盐酸克伦特罗,白色或类白色的结晶粉末,无臭、味苦,熔点161℃,溶于水、乙醇,微溶于丙酮,不溶于乙醚.其结构简式如图.有关瘦肉精的说法不正确的是( )
食品安全是现今百姓生活中热议问题之一,瘦肉精学名盐酸克伦特罗,白色或类白色的结晶粉末,无臭、味苦,熔点161℃,溶于水、乙醇,微溶于丙酮,不溶于乙醚.其结构简式如图.有关瘦肉精的说法不正确的是( )| A. | 化学式为C12H18ONCl2 | |
| B. | 遇FeCl3溶液发生显色反应 | |
| C. | 属于芳香族化合物 | |
| D. | 可以发生取代、加成、水解、酯化、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com