
某同学用如图所示装置(固定、加热仪器和橡胶管略)进行有关氨制取的实验探究,回答下列问题.
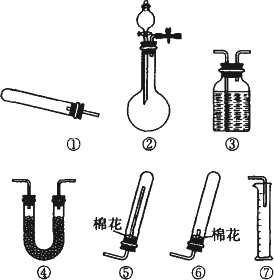
(1)若用装置①制取NH3,其反应的化学方程式为________;若要测定生成的NH3的体积,则必须选择的装置是________(填装置序号),装置中所盛试剂应具有的性质是________.
(2)若用装置②制取并收集干燥的NH3,烧瓶内装的试剂是________,分液漏斗中装的试剂是________,收集装置应选择________(填装置序号).证明氨已收集满的操作是________.检验装置②的气密性的方法是________.
(3)若用下列各种试剂组合(其他条件相同)进行制取氨的对比实验,测出氨的体积(标准状况)如下表:
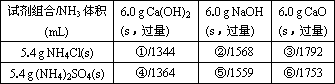
从表中数据分析,实验室制氨的产率最高的是________(填序号).其原因是________.
(1)2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;③⑦;氨难溶于该试剂,该试剂不易挥发且不与氨反应.
2NH3↑+CaCl2+2H2O;③⑦;氨难溶于该试剂,该试剂不易挥发且不与氨反应.
(2)CaO或NaOH或碱石灰;浓氨水;⑤.用湿润的红色石蕊试纸靠近试管口,若试纸变蓝则证明已收集满;在橡胶管处接上导气管,关闭分液漏斗活塞,打开止水夹,将导气管末端插入水槽中,用热毛巾捂着烧瓶(或用酒精灯微热),导气管末端有气泡冒出,移开热毛巾(或停止加热)一段时间,导气管末端有一段水柱(或关闭装置②的止水夹和分液漏斗活塞,从分液漏斗的上端注入一定量的水,打开分液漏斗活塞,若漏斗中的水滴入烧瓶中的速率逐渐减慢至不再滴入,说明装置气密性良好).
(3)⑥;NH4Cl受热易分解,生成的部分NH3和HCl又重新结合生成NH4Cl,而用NaOH和Ca(OH)2反应产生的水较多,吸收的NH3较多,所以用CaO和(NH4)2SO4反应产率最高.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学用如图所示装置探究SO2的性质及其有关实验.
某同学用如图所示装置探究SO2的性质及其有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学用如图所示装置探究SO2的性质及其有关实验.
某同学用如图所示装置探究SO2的性质及其有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学用如图所示装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.
某同学用如图所示装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学用如图所示装置制取乙酸乙酯.在试管甲中加入适量的乙醇、浓硫酸和冰醋酸,并加热3min~5min.请回答:
某同学用如图所示装置制取乙酸乙酯.在试管甲中加入适量的乙醇、浓硫酸和冰醋酸,并加热3min~5min.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com