
【题目】常温下,向盛有1 L 0.1 mol·L-1NaHSO4溶液的烧杯中不断滴加0.05 mol·L-1的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如下图所示,下列说法不正确的是

A. A点时pH=1
B. 恰好完全沉淀时Ba(OH)2的体积为2 L
C. B点时,溶液中的离子浓度关系为c(Na+)>c(SO![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
D. C点时pH=14
【答案】D
【解析】0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,pH=1,A正确;往NaHSO4溶液中滴加Ba(OH)2反应过程为①2NaHSO4+Ba(OH)2===BaSO4↓+Na2SO4+2H2O(中性),继续加入Ba(OH)2溶液,Na2SO4+Ba(OH)2===BaSO4↓+2NaOH,总反应为②NaHSO4+Ba(OH)2===BaSO4↓+NaOH+H2O,故恰好完全沉淀时,n(NaHSO4)=n[Ba(OH)2],由此求出Ba(OH)2体积为2 L,B正确;B点时发生反应①,溶质为Na2SO4,pH=7,C正确;C点时发生反应②,n(OH-)=1×0.1=0.1 mol,但溶液体积为3 L,
c(OH-)=![]() ≈0.033 mol·L-1,pH≠14,D错
≈0.033 mol·L-1,pH≠14,D错


科目:高中化学 来源: 题型:
【题目】(I)工业上过氧化氢是重要的氧化剂和还原剂。常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:____________________________。
(2)同学们用0.1000mol/L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①在该反应中,H2O2被_________(填“氧化”或“还原”)。
②滴定到达终点的现象是____________________________。
③用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为__________mol/L-1。
(II)医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。测定含量如下:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀疏酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(1)滴定时,用_____(填酸或碱)式滴定管装KMnO4溶液。
(2)下列操作会引起测定结果偏高的是______。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.锥形瓶未用待测液润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g) △H>0,平衡体系中气体的平均摩尔质量(
2NO2(g) △H>0,平衡体系中气体的平均摩尔质量(![]() )在不同温度下随压强的变化曲线如图所示。下列说法正确的是
)在不同温度下随压强的变化曲线如图所示。下列说法正确的是

A. 温度:T1<T2 B. 平衡常数:K(a)=K(b)<K(c)
C. 反应速率:v(b)>v(a) D. 当![]() =69g/mol时,n(NO2):n(N2O4)=2:1
=69g/mol时,n(NO2):n(N2O4)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.2molN2O4(g)充入2L的恒容密闭容器中,间隔一定时间后对该容器内各物质的物质的量进行测定,得到如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
N(N2O4)/mol | 0.20 | n1 | 0.10 | n3 | n4 |
N(NO2)/mol | 0.00 | 0.12 | n2 | 0.24 | 0.24 |
(1)该反应的平衡常数表达式为___________________________,由表中数据分析可得,n1=____mol,n3=________________mol;
(2)在上述条件下,从0到40s内NO2的平均反应速率为___________________;
(3)该反应达到化学平衡后,下列改变可使N2O4浓度增大的是_____(填序号);
A.增大容器的容积 B.向容器中充入一定量的NO2
C.向容器中再充入一定量的N2O4 D.向容器中充入一定量的He(g)
(4)在下图中画出此反应中N2O4的浓度随时间变化的曲线_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置和方法进行相应实验,能达到实验目的的是
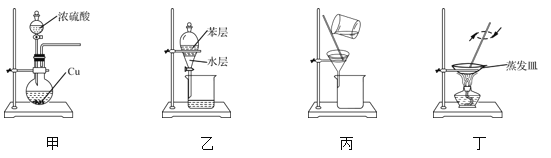
A. 用装置甲制备SO2
B. 用装置乙从碘水溶液中萃取碘
C. 用装置丙除去粗盐溶液中混有的KCl杂质
D. 用装置丁蒸干溶液获得(NH4)2CO3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示;

回答下列问题:
(1)A的结构简式为_____________________。
(2)由乙醇生产C的化学反应类型为_____________________。
(3)E是一种常见的塑料,其化学名称是_____________________。
(4)由乙醇生成F的化学方程式为__________________________________。
(5)写出A生成B的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是

A. X分子只存在2个手性碳原子
B. X分子能发生氧化、取代、消去反应
C. X分子中所有碳原子可能在同一平面上
D. 1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】那可汀是一种药物,该药适用于刺激性干咳病人服用,无成瘾性。化合物I是制备该药物的重要中间体,合成路线如下:

(1)化合物A中的官能团名称为________________(写两种)。
(2)设计反应A→B的目的为________________________________。
(3)化合物C的分子式为C10H11O4I,写出C的结构简式:________________________。
(4)化合物I的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:____________________。
①分子中含有硝基(—NO2)且直接连在苯环上;②分子中只有3种不同化学环境的氢。
(5)写出以 和
和 为原料制备
为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组的电极材料和电解液,不能组成原电池的是( )
A. 铜片、石墨棒,蔗糖溶液B. 锌片、石墨棒,硫酸铜溶液
C. 锌片、铜片,稀盐酸D. 铜片、银片,硝酸银溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com