
| A. | 氯气、二氧化硫都能使品红溶液褪色,它们的漂白原理相同 | |
| B. | 纯净的晶体硅是现代光学及光纤制品的基本原料 | |
| C. | 用丁达尔效应可鉴别FeCl3溶液和Fe(OH)3胶体 | |
| D. | NH3的水溶液可以导电,所以NH3是电解质 |
分析 A.氯气的漂白原理:氯气与水反应生成次氯酸,次氯酸具有强氧化性;二氧化硫的漂白原理:有色物质结合成无色物质;
B.纯净的二氧化硅良好的折光性;
C.胶体具有丁达尔现象,溶液不具有丁达尔现象;
D.水溶液中或熔融状态导电的化合物为电解质,本身能电离出自由移动的离子.
解答 解:A.氯气与水反应生成次氯酸,次氯酸具有强氧化性,使品红氧化褪色;二氧化硫与有色物质结合成无色物质,使品红褪色,加热恢复原来的颜色,两者漂白原理不同,故A错误;
B.纯净的二氧化硅良好的折光性,是现代光学及光纤制品的基本原料,晶体硅是集成电路和太阳能电池板的原料,故B错误;
C.丁达尔效应是胶体特有的性质,可区分胶体和溶液,故C正确;
D.NH3的水溶液可以导电,是因为氨气和水反应生成了电解质一水合氨,氨气本身不能电离出离子,所以NH3是非电解质,故D错误;
故选C.
点评 本题考查了物质性质应用,电解质概念的理解分析,主要是氯气、二氧化硫、二氧化硅、氨气等物质性质的理解应用,题目较简单.


科目:高中化学 来源: 题型:选择题
 用下列装置(尾气处理已略去)进行相关实验,能实现实验目的是( )
用下列装置(尾气处理已略去)进行相关实验,能实现实验目的是( )| 实验目的 | a中试剂 | b中试剂 | c中试剂 | |
| A | 比较H2CO3、H2SiO3 的酸性 | 醋酸溶液 | 碳酸钠 | 硅酸钠溶液 |
| B | 比较Cl2、I2的 氧化性 | 浓盐酸 | 高锰酸钾 | 碘化钾溶液 |
| C | 制备NaHCO3 | 盐酸 | 大理石 | 饱和碳酸钠溶液 |
| D | 证明C2H2有还原性 | 饱和食盐水 | 电石 | 酸性高锰酸钾溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
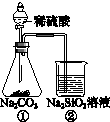
| A. | ①和②中发生的反应均为复分解反应 | |
| B. | 向Na2SiO3饱和溶液中滴酚酞溶液无明显现象 | |
| C. | 一段时间后②中有胶冻状物质生成 | |
| D. | 该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 实验操作 | 实验现象 |
| 甲 | ①取少量粉末,加入过量浓硝酸 ②向上述溶液中加入几滴NaCl溶液 | 粉末溶解,有红棕色气体产生 有白色沉淀生成 |
| 乙 | ③取少量粉末,加入足量NaOH溶液 ④向上述溶液中逐滴加入稀盐酸 ⑤继续加入过量的稀盐酸 | 粉末溶解,有气泡产生 有白色沉淀生成 白色沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应必然伴随能量的变化 | |
| B. | 我国目前使用的主要能源是化石能源 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 化学反应一定有化学键的断裂与形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
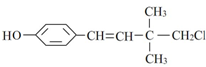 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 有顺反异构 | |
| B. | 可以和浓溴水发生取代反应和加成反应 | |
| C. | 可以发生加聚反应、水解反应和消去反应 | |
| D. | 1mol该化合物最多能与4 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=4.3的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | 浓度为0.2mol/L的CH3COOH溶液和农地为0.1mol/L的NaOH溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] | |
| C. | 醋酸溶液加少量水稀释,$\frac{c(C{H}_{3}COOH)}{{c}^{2}({H}^{+})}$几乎不变 | |
| D. | amol/LCH3COOH溶液与bmol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CH3COO-),则一定有a≤b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com