
| A. | 反应①中的能量变化如图所示: | |
| B. | CO(g)+2H2 (g)═CH3OH(g)△H<-90.5kJ•mol-1 | |
| C. | 2CH4 (g)+3O2 (g)═2CO(g)+4H2O(g)△H<-71.0kJ•mol-1 | |
| D. | 2CH4 (g)+$\frac{1}{2}$O2 (g)═CH3OH( l))△H=-126.0kJ•mol-1 |
分析 A、反应①为放热反应,即反应物总能量高于生成物总能量;
B、与反应②比较,1molCH3OH(g)能量高于1molCH3OH(l),根据能量守恒定律判断;
C、氢气燃烧还要放出热量,据此解答即可;
D、根据已知方程式结合盖斯定律分析计算.
解答 解:A、D、已知①2CH4(g)+O2(g)=2CO(g)+4H2(g);△H=-71kJ•mol-1,该反应为放热反应,所以反应物的能量总和大于生成物能量总和,故A正确;
B、A、与反应②比较,1molCH3OH(g)能量高于1molCH3OH(l),反应物的总能量相同,根据能量守恒定律可知该反应放出的热量小于反应②,故△H>-90.5kJ/mol,故B错误;
C、2CH4 (g)+O2 (g)═2CO(g)+4H2(g)△H=-71.0 kJ•mol-1,①
4H2 (g)+2O2 (g)═4H2O(l)△H=a<0kJ•mol-1,②
①+②得:2CH4 (g)+3O2 (g)═2CO(g)+4H2O(g)△H=-71.0 kJ•mol-1+a<=-71.0 kJ•mol-1,故C正确;
D、已知①2CH4(g)+O2(g)=2CO(g)+4H2(g);△H=-71kJ•mol-1
②CO(g)+2H2(g)=CH3OH(l);△H=-90.5kJ•mol-1,
根据盖斯定律可知:$\frac{1}{2}$①+②得到方程CH4(g)+$\frac{1}{2}$O2(g)═CH3(OH)(l)△H=-126kJ•mol-1,故D正确;
故选B.
点评 本题考查反应热的计算、盖斯定律的应用、热化学方程式书写、燃料电池等,难度中等,侧重于对反应原理的应用的考查.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:解答题

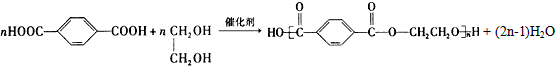 .
.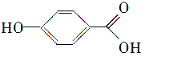 .
.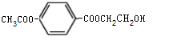 、
、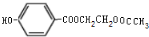 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 阶段/含量%/成分 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
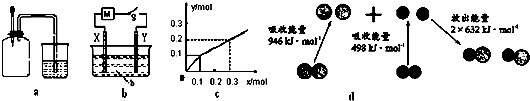
| A. | 如图a所示,集气瓶内充满Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,并可能充满集气瓶 | |
| B. | Pt为电极,电解含0.10 mol M+和0.1 mol N3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+ | |
| C. | 如图b所示,X为铁棒,Y为铜棒,M为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入M | |
| D. | 图d为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N≡N的键能为946kJ/mol,其热化学方程式为 N2(g)+O2(g)═2NO(g)△H=-180 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,已知这四种元素中只有一种是金属元素.下列判断正确的是( )
A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,已知这四种元素中只有一种是金属元素.下列判断正确的是( )| A. | C的氯化物与水反应,可生成白色烟雾 | |
| B. | A的氧化物对应的水化物一定为强酸 | |
| C. | D的最高价氧化物对应的水化物能和D的氢化物发生反应生成盐 | |
| D. | 向含B元素的盐溶液中滴加碳酸氢钠溶液,可能不出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
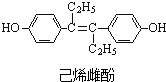
| A. | 与NaOH反应可生成化学式为C18H18O2Na2的化合物 | |
| B. | 聚己烯雌酚含有顺式和反式两种结构 | |
| C. | 1mol己烯雌酚最多可与7molH2发生加成反应 | |
| D. | 形成高分子 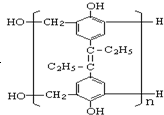 的单体中有己烯雌酚 的单体中有己烯雌酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用装置精炼铜,则b极为精铜,电解质溶液为CuSO4溶液 | |
| B. |  装置的总反应是Cu+2Fe3+=Cu2++2Fe2+ | |
| C. |  装置中钢闸门应与外接电源的负极相连 | |
| D. |  装置中的铁钉浸入浓硫酸中几乎没被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 元素的离子半径A<B<C<E | |
| B. | 工业上利用电解C的氯化物溶液的方法制备单质C | |
| C. | D的气态氢化物和最高价氧化物的水化物可能发生氧化还原反应 | |
| D. | D与C,A与D形成的化合物中化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤 | 向 MgCl2溶液中滴加NaOH溶液 | 向有白色沉淀的溶液中滴加FeCl3溶液 | 静置 |
| 现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com