
| 1 |
| 2 |
| 3 |
| 2 |
| 0.5×0.5 |
| 1.5×0.5 |
| 1 |
| 3 |


科目:高中化学 来源: 题型:
| 阳离子 | K+、Ag+、Na+、Ba2+、Fe2+、Al3+ |
| 阴离子 | Cl-、OH-、AlO2-、NO3-、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01mol?L-1醋酸溶液 |
| B、0.02mol?L-1醋酸与0.01mol?L-1NaOH溶液等体积混合液 |
| C、0.03mol?L-1醋酸与0.01mol?L-1NaOH溶液等体积混合液 |
| D、pH=2的盐酸与0.01mol?L-1NaOH溶液等体积混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、缺铁会患贫血症 |
| B、为防治佝偻病,过量补钙 |
| C、摄入糖分不足,会患低血糖 |
| D、缺碘人群可多食用海带、虾皮等含碘丰富的食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
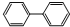 ,下列有关联苯的说法中正确的是( )
,下列有关联苯的说法中正确的是( )| A、分子中含有6个碳碳双键 |
| B、联苯的一硝基取代产物的3种 |
| C、它容易发生加成反应、取代反应,容易被强氧化剂氧化 |
D、它和蒽(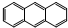 )同属于芳香烃,两者互为同系物 )同属于芳香烃,两者互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷与氯气在光照条件下的反应 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、己烷与溴水混合振荡,静置后溴水层褪色 |
| D、在催化剂作用下,乙烯和水反应生成乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-(6-3n) |
| B、-(8-n) |
| C、-(12-3n) |
| D、-(14-5n) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com