
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
���� ��1����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���ݴ���д��ע����塢��Һ���Ũ��Ϊ����������Ҫд���塢��Һ�壻
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ��
��2�����CO��ƽ��ת���ʣ�Ӧʹƽ��������Ӧ�ƶ�������������CO�����������ѡ�����ƽ���ƶ�ԭ��������
��3������Ũ��������ȶ��Ե�ƽ�ⳣ���Ĵ�С��ϵ�ж�ƽ���ƶ�������ƽ��ʱCO�����ʵ����仯Ϊnmol����������ʽ��ʾ��ƽ��ʱCO��CO2�����ʵ�������ѧ����������1���������ʵ�������Ũ�ȴ���ƽ�ⳣ������n��ֵ����������CO2��Ũ�ȱ仯��������v=$\frac{��c}{��t}$����v��CO2����������ת���ʶ������CO��ת���ʣ�
��� �⣺��1����Ӧ$\frac{1}{3}$Fe2O3��s��+CO��g��?$\frac{2}{3}$Fe��s��+CO2��g����ƽ�ⳣ��K=$\frac{c��C{O}_{2}��}{c��CO��}$��
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ��$\frac{c��C{O}_{2}��}{c��CO��}$������
��2��A�����ǹ��壬����Fe��������Ӱ��ƽ���ƶ���CO��ƽ��ת���ʲ��䣬��A����
B���������ǹ��壬����Fe2O3��������Ӱ��ƽ���ƶ���CO��ƽ��ת���ʲ��䣬��B����
C���Ƴ�����CO2��ƽ��������Ӧ�ƶ���CO��ƽ��ת��������C��ȷ��
D��������ʵĴ�����ƽ�ⲻ�ƶ�����D����
E����Ӧǰ����������ʵ������䣬��С�������ݻ�������ѹǿƽ�ⲻ�ƶ���CO��ƽ��ת���ʲ��䣬��E����
F���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ����߷�Ӧ�¶ȣ�ƽ�����淴Ӧ�ƶ���CO��ƽ��ת���ʽ��ͣ���F����
��ѡC��
��3����һ���ݻ�Ϊ1L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��2.0mol����ʱŨ����Ϊ��Qc=$\frac{\frac{2.0}{1L}}{\frac{2.0}{1L}}$=1��K=4�����ʱƽ�����������ƶ���V��������V���棩��
��ƽ��ʱCO�����ʵ����仯Ϊnmol����
$\frac{1}{3}$Fe2O3��s��+CO��g��?$\frac{2}{3}$Fe��s��+CO2��g��
��ʼ��mol����2 2
�仯��mol����n 2+n
ƽ�⣨mol����2-n 2+n
����$\frac{\frac{2+n}{V}}{\frac{2-n}{V}}$=4��
��ã�n=1.2��
����v��CO2��=$\frac{\frac{1.2mol}{1L}}{5min}$=0.24 mol•L-1•min-1��
CO��ƽ��ת����Ϊ��$\frac{1.2mol}{2mol}$��100%=60%��
�ʴ�Ϊ������0.24mol•L-1•min-1��60%��
���� ���⿼�黯ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ��漰��ѧ��Ӧ���ʼ��㡢ƽ�ⳣ������ѧƽ�⼰��Ӱ���֪ʶ��ע�����ջ�ѧ��Ӧ���ʡ���ѧƽ�ⳣ���ĸ������ʽ������������ѧ���Ļ�ѧ����������


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
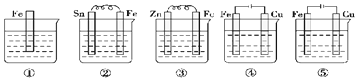
| A�� | �ݢڢ٢ۢ� | B�� | �ۢڢݢܢ� | C�� | �ݢܢۢڢ� | D�� | �ݢڢ٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ������������Һ��ϡ���� | B�� | ˮ������������Һ��ϡ����? | ||
| C�� | ˮ����������Һ��ϡ���� | D�� | ˮ������������Һ��ϡ����? |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
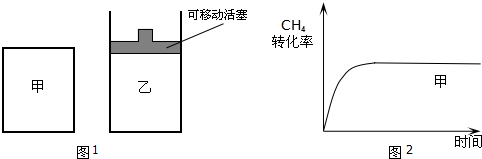
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | �������������۵Ĵ�����Ϊ4 |
| X | �����������Ǵ�����������2�� |
| Y | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯���ˮ��Һ�ʼ��� |
| Z | ���������+7�� |
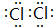 ��Y���⻯���ˮ��Һ�Լ��Ե�ԭ��ΪNH3+H2O?NH3•H2O?NH4++OH-�������ӷ���ʽ��ʾ����
��Y���⻯���ˮ��Һ�Լ��Ե�ԭ��ΪNH3+H2O?NH3•H2O?NH4++OH-�������ӷ���ʽ��ʾ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
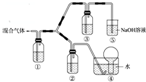 A��B��C��D��E���ֶ�����Ԫ�أ�A��B��C��D��E�ֱ����Ԫ�ط��ţ������ǵ�ԭ��������������A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�BԪ������������Ӧ��ˮ���������⻯�ﷴӦ����һ����X��D��Aͬ���壬����Eͬ���ڣ�EԪ��ԭ�ӵ��������������������������$\frac{3}{4}$����C��Eͬ���壮
A��B��C��D��E���ֶ�����Ԫ�أ�A��B��C��D��E�ֱ����Ԫ�ط��ţ������ǵ�ԭ��������������A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�BԪ������������Ӧ��ˮ���������⻯�ﷴӦ����һ����X��D��Aͬ���壬����Eͬ���ڣ�EԪ��ԭ�ӵ��������������������������$\frac{3}{4}$����C��Eͬ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
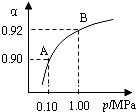 ��ҵ������Ϊԭ���������ᣬ��֪4g����ȫ�ɷų�aKJ���ȣ���
��ҵ������Ϊԭ���������ᣬ��֪4g����ȫ�ɷų�aKJ���ȣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaOCl2 | B�� | ��NH4��2Fe��SO4��2 | C�� | Na3A1F6 | D�� | Cu2��OH��2CO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com