
”¾ĢāÄæ”æijĶ¬Ń§Óū×ö1-Āȶ”ĶéµÄĖ®½āŹµŃ飬²¢¼ģŃéĘäÖŠµÄĀČŌŖĖŲ”£ŹµŃé¹ż³ĢČēĻĀ£ŗ
ČēĶ¼ĖłŹ¾£¬ŌŚ“óŹŌ¹ÜÖŠ¼ÓČė5 mL 1 mol”¤L£1NaOHČÜŅŗŗĶ5 mL 1-Āȶ”Ķé(1-Āȶ”ĶéµÄ·ŠµćĪŖ77”«78 ”ę£¬ĆܶČĪŖ0.886 g”¤cm£3 £¬ Ņ×Č¼)”£Ė®Ō”¼ÓČČøĆŹŌ¹Ü10 minŅŌÉĻ£¬²¢æŲÖĘ¼ÓČČĪĀ¶ČŌŚ70”«80 ”ę”£Č”2Ö§Š”ŹŌ¹Ü£¬ø÷¼ÓČėŌ¼1 mLÓÉ2%µÄAgNO3ŗĶ3 mol”¤L£1ĻõĖį°“1”Ć1±ČĄż×é³ÉµÄ»ģŗĻČÜŅŗ£¬ÓĆ½ŗĶ·µĪ¹ÜĪüČ”¼ÓČČŗó“óŹŌ¹ÜÄŚµÄÉĻ²ćČÜŅŗ£¬½«“Ė“ż²āŅŗÖšµĪ¼ÓČėĘäÖŠŅ»Ö§Š”ŹŌ¹ÜÖŠ£¬ÓėĮķŅ»Ö§Ī“¼Ó“ż²āŅŗµÄŠ”ŹŌ¹ÜÄŚČÜŅŗĻą±Č£¬ÓŠ°×É«µÄ»ė×ĒĪļ³öĻÖ£¬ĖµĆ÷1-Āȶ”ĶéÓėNaOHČÜŅŗ·“Ó¦ÓŠCl£Éś³É£¬“Ó¶ųÖ¤Ć÷ĮĖ1-Āȶ”ĶéÖŠŗ¬ÓŠĀČŌŖĖŲ”£
Ēė»Ų“š£ŗ
£Ø1£©ĒėŠ“³ö1-Āȶ”ĶéĖ®½āµÄ»Æѧ·½³ĢŹ½£ŗ
ӣ
£Ø2£©ŹŌ¹ÜÉĻ·½µÄ²£Į§µ¼¹ÜµÄ×÷ÓĆĪŖ”£
£Ø3£©¼ģŃéCl£Ź±£¬ÓĆĻõĖįĖį»ÆAgNO3ČÜŅŗµÄÄæµÄŹĒ
ӣ
£Ø4£©øĆ×°ÖĆŹĒÓŠ»ś»ÆѧŹµŃéÖŠ³£ÓƵÄŅ»Ģ××°ÖĆ£¬ŹµŃéŹŅÖŠ£¬æÉŅŌŹ¹ÓĆÉĻŹö×°ÖĆÖʱøµÄŹĒ£Ø£©(ĢīŠņŗÅ)”£
A.Ļõ»ł±½
B.ŅŅĻ©
C.ŅŅĖįŅŅõ„
D.äå±½
”¾“š°ø”æ
£Ø1£©CH3CH2CH2CH2Cl£«NaOH ![]() CH3CH2CH2CH2OH£«NaCl
CH3CH2CH2CH2OH£«NaCl
£Ø2£©ĄäÄż»ŲĮ÷£¬±£³ÖÓė“óĘųĻąĶØ
£Ø3£©ÅųżĒāŃõøłĄė×ÓµÄøÉČÅ
£Ø4£©A
”¾½āĪö”æ(1)ŌŚ1-Āȶ”ĶéĖ®½ā¹ż³ĢÖŠ·¢ÉśĮ½øö·“Ó¦£¬Ź×ĻČĖ®½āÉś³É1-¶”“¼ÓėHCl£¬½ų¶ųHClÓėNaOHČÜŅŗ·“Ó¦£¬“Ł½ųĮĖ1-Āȶ”ĶéµÄĖ®½ā”£(2)ÓÉÓŚ1-Āȶ”ĶéµÄ·ŠµćÖ»ÓŠ77”«78 ”ę£¬ŌŚ¼ÓČČŹ±ČŻŅ×»Ó·¢£¬µ«ÓÖ²»ÄÜĆÜ·ā£¬ÉĻŹö×°ÖĆÓŠŠ§µŲ½ā¾öĮĖÕāøöĪŹĢā”£Ņ»·½Ćę£¬²£Į§µ¼¹ÜÓė“óĘųĻąĶØ£¬²»ÖĀÓŚ³öĻÖĪ£ĻÕ£¬¶ų¼ÓČČŹ±£¬Ņ©Ę·ĻņÉĻ»Ó·¢µÄ¹ż³ĢÖŠÓöµ½æÕĘųĄäÄż£¬ÓÖÖŲŠĀ±ä³ÉŅŗĢ壬»ŲĮ÷µ½ŹŌ¹ÜÖŠ£¬¼ĢŠų²Ī¼Ó·“Ó¦”£(3)ÓĆĻõĖįĖį»ÆAgNO3ČÜŅŗµÄÄæµÄ£¬ŹĒÖŠŗĶ“ż²āŅŗÖŠµÄNaOH£¬·ĄÖ¹NaOHÓėAgNO3·“Ӧɜ³É³Įµķ£¬Ó°ĻģŹµŃ銧¹ū”£(4)ŹµŃéŹŅÖĘČ”Ļõ»ł±½Ź±ŠėŌŚ50”«60 ”ęĢõ¼žĻĀ½ųŠŠ£¬¶ų·“Ó¦»ģŗĻĪļÖŠµÄĻõĖį”¢±½¶¼ČŻŅ×»Ó·¢£¬ÓėÉĻŹöŹµŃéĢõ¼žĻąĖĘ£¬æÉŅŌŹ¹ÓĆÉĻŹö×°ÖĆ”£ÖĘŅŅĻ©ŠčŌŚ170 ”ęĢõ¼žĻĀ½ųŠŠ£¬²»ÄÜÓĆĖ®Ō”¼ÓČČ£¬ÖĘŅŅĖįŅŅõ„Ź±Ö±½Ó¼ÓČČ¼“æÉ”£ÖĘäå±½²»ÓĆ¼ÓČČ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²¹Ģś¼ĮÖŠĢśŌŖĖŲµÄŗ¬ĮæŹĒÖŹ¼ģ²æĆÅŗāĮæĘäÖŹĮæµÄÖŲŅŖÖø±ź£¬ŹµŃéÖ÷ŅŖ°üĄØČēĻĀ²½Öč£ŗ
¢ŁÅäÖĘ0.01 mol”¤L£1”¢0.008 mol”¤L£1µČŅ»ĻµĮŠÅØ¶ČµÄ[Fe(SCN)6]3£(ŗģÉ«)±ź×¼±ČÉ«Ņŗ”£
¢ŚŃłĘ·“¦Ąķ£ŗ![]()
¢Ū×¼Č·ĮæČ”Ņ»¶ØĢå»żµÄ“ż²āŅŗÓŚ±ČÉ«¹ÜÖŠ£¬¼ÓČėÉŌ¹żĮæµÄKSCNČÜŅŗ£¬²¢Ļ”ŹĶµ½10 mL”£
¢Ü±ČÉ«£¬Ö±µ½ÓėєȔµÄ±ź×¼ŃÕÉ«Ņ»ÖĀ»ņĻą½ü¼“æÉ”£
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÅäÖĘ100 mL 0.01 mol”¤L£1ČÜŅŗ£¬ŠčŅŖµÄ²£Į§ŅĒĘ÷ÓŠ£ŗÉÕ±”¢²£Į§°ō£¬»¹ŠčŅŖ£ŗ”¢”£
£Ø2£©²½Öč¢ŚĶŃÉ«¹ż³Ģ°üĄØ¼ÓČė£ŗ(ĢīĶŃÓŠ»śÉ«ĖŲµÄĪüø½¼ĮĆū³Ę)”ś½Į°čÖó·Š”śĄäČ“”ś(Ģī²Ł×÷)”£
£Ø3£©±ČÉ«·ØČ·¶Ø“ż²āŅŗµÄÅØ¶ČµÄŌĄķŹĒ”£
£Ø4£©ČōĘä²¹Ģś¼ĮŹĒÓÉČéĖį[CH3CH(OH)COOH]ÓėĢś·Ū×÷ÓĆÉś³ÉµÄ£¬ĒėŠ“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ£Ø £©
A.ŌŚNaClOČÜŅŗÖŠĶØČė¹żĮæSO2ĘųĢå£ŗClO©+H2O+SO2ØTHClO+HSO ![]()
B.ÓĆĻ”ĒāµāĖįČÜŅŗ³żČ„ĢśÖĘĘ·±ķĆęµÄĢśŠā£ŗFe2O3+6H+ØT2Fe3++3H2O
C.NaHCO3ÓėÉŁĮæµÄCa£ØOH£©2ČÜŅŗ·“Ó¦£ŗCa2++2OH©+2HCO ![]() ØTCaCO3”ż+2H2O+CO
ØTCaCO3”ż+2H2O+CO ![]()
D.10mL 0.5mol/LµÄĆ÷·ÆČÜŅŗÓė20mL 0.5mol/L Ba£ØOH£©2ČÜŅŗ»ģŗĻ·“Ó¦£ŗ3Ba2++6OH©+2Al3++3SO ![]() ØT3BaSO4”ż+2Al£ØOH£©3”ż
ØT3BaSO4”ż+2Al£ØOH£©3”ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧÓėÉś»ī”¢Éē»įĆÜĒŠĻą¹Ų£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.Ņ½Ōŗ³£ÓĆ75%µÄ¾Ę¾«×÷Ļū¶¾¼Į
B.Ķ؊ŹāĄĀµÄÖ÷ŅŖ³É·ÖŹĒ¾§Ģå¹č£¬Ģ«ŃōÄܵē³ŲµÄ²ÄĮĻÖ÷ŅŖŹĒSiO2
C.ĀČĘų”¢³ōŃõ”¢øßĢśĖį¼Ų¶¼ŹĒ³£ÓƵÄ×ŌĄ“Ė®Ļū¶¾¼Į
D.»īŠŌĢś·ŪæÉÓĆ×÷æ¹Ńõ»Æ¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠĖȤŠ”×éĪŖŃéÖ¤ČÕ³£Éś»īÓƵĻš²ńĶ·ÉĻŗ¬ÓŠKClO3”¢MnO2”¢S£¬Éč¼ĘĮĖŅŌĻĀŹµŃéĮ÷³ĢĶ¼£ŗ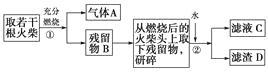
Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©ĪŖŃéÖ¤ĘųĢåA£¬°“ČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£ŗČōÄܹŪ²ģµ½µÄĻÖĻ󣬼“æÉÖ¤Ć÷»š²ńĶ·ÉĻŗ¬ÓŠSŌŖĖŲ”£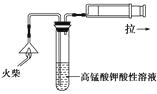
£Ø2£©²½Öč¢ŚµÄŹµŃé²Ł×÷×°ÖĆČēĶ¼ĖłŹ¾£¬øĆ²Ł×÷µÄĆū³ĘŹĒ £¬ Ę乤×÷ŌĄķŹĒ”£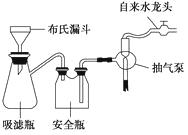
£Ø3£©ŅŖÖ¤Ć÷»š²ńĶ·ÖŠŗ¬ÓŠClŌŖĖŲµÄŗóŠųŹµŃé²½ÖčŹĒ£æ
£Ø4£©ÓŠŃ§ÉśĢį³ö¼ģŃ黚²ńĶ·ÉĻKClO3µÄĮķŅ»Ģ׏µŃé·½°ø£ŗ
ÓŠ¹ŲµÄĄė×Ó·½³ĢŹ½ĪŖ £¬
ÓŠČĖĢį³öÉĻŹö·½·ØÖŠ³öĻÖ°×É«³Įµķ²¢²»Äܳä·ÖĖµĆ÷»š²ńĶ·ÉĻKClO3µÄ“ęŌŚ£¬ĘäĄķÓÉŹĒ”£
£Ø5£©øĆŠ”×é²Ā²āĀĖŌüD¶ŌĖ«ŃõĖ®·Ö½āÖĘŃõĘųµÄĖŁĀŹ»į²śÉśŅ»¶ØµÄÓ°Ļģ£¬Éč¼Ę²¢½ųŠŠĮĖŅŌĻĀ5“ĪŹµŃ锣
ŹµŃé“ĪŹż | H2O2ČÜŅŗÖŹĮæ·ÖŹż/% | H2O2ČÜŅŗÓĆĮæ/mL | ĪļÖŹDÓĆĮæ/g | ·“Ó¦ĪĀ¶Č/”ę | ŹÕ¼ÆĘųĢåĢå»ż/mL | ĖłŠčŹ±¼ä/s |
¢Ł | 30 | 5 | 0 | 85 | 2 | 3.8 |
¢Ś | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
¢Ū | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
¢Ü | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
¢Ż | 30 | 5 | 0 | 55 | 2 | 10.5 |
ÓÉÉĻ±ķæÉÖŖ£¬ŹµŃé¢ŁŗĶ¢ŻÄÜÖ¤Ć÷ĪĀ¶ČŌ½øߣ¬»Æѧ·“Ó¦ĖŁĀŹŌ½æģ£¬ŹµŃéŗĶÄÜÖ¤Ć÷ĪļÖŹDµÄÓĆĮæŌ½“󣬷“Ó¦ĖŁĀŹŌ½æģ”£
£Ø6£©Š“³ö²½Öč¢ŁÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓÉFe2O3”¢Fe”¢CuO”¢C”¢AlÖŠµÄ¼øÖÖĪļÖŹ×é³ÉµÄ»ģŗĻ·ŪÄ©£¬Č”ѳʷ½ųŠŠĻĀĮŠŹµŃé£Ø²æ·Ö²śĪļĀŌČ„£©”£¹ŲÓŚ»ģŗĻ·ŪÄ©µÄ×é³ÉÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©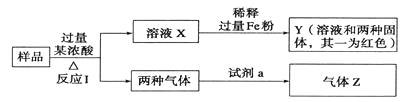
A.Ņ»¶Øŗ¬CuOŗĶC
B.Ņ»¶Øŗ¬Fe2O3”¢CuOŗĶC
C.Ņ»¶Øŗ¬CuOŗĶC£¬Ņ»¶Ø²»ŗ¬Al
D.ĘųĢåZĪŖ“æ¾»Īļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅ³£ÓĆÅØŃĪĖįÓė¶žŃõ»ÆĆĢ·“Ó¦Ą“ÖĘȔɣĮæĀČĘų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗMnO2£«4HCl(ÅØ)![]() MnCl2£«Cl2”ü£«2H2O”£ĻČ½«Ņ»¶ØĮæµÄ¶žŃõ»ÆĆĢČܽāŌŚ200mLÅØŃĪĖįÖŠ£¬µ±·“Ӧɜ³É8.96L(±źæöĻĀ)Cl2Ź±£¬²āµĆŹ£ÓąČÜŅŗÖŠŃĪĖįµÄÅضČĪŖ2mol/L£Ø¼ŁÉč·“Ó¦Ē°ŗóČÜŅŗµÄĢå»ż²»±ä£©”£»Ų“šĻĀĮŠĪŹĢā£ŗ
MnCl2£«Cl2”ü£«2H2O”£ĻČ½«Ņ»¶ØĮæµÄ¶žŃõ»ÆĆĢČܽāŌŚ200mLÅØŃĪĖįÖŠ£¬µ±·“Ӧɜ³É8.96L(±źæöĻĀ)Cl2Ź±£¬²āµĆŹ£ÓąČÜŅŗÖŠŃĪĖįµÄÅضČĪŖ2mol/L£Ø¼ŁÉč·“Ó¦Ē°ŗóČÜŅŗµÄĢå»ż²»±ä£©”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŃĪĖįŌŚ·“Ó¦ÖŠ±ķĻÖ³öµÄŠŌÖŹĪŖ___________________”£
£Ø2£©Š“³öÉĻŹöÖĘČ”Cl2µÄĄė×Ó·½³ĢŹ½£ŗ______________________________ ”£
£Ø3£©¼ĘĖć·“Ó¦ŗÄÓĆMnO2µÄÖŹĮæĪŖ_________g,±»Ńõ»ÆµÄHClµÄĪļÖŹµÄĮæĪŖ______ mol£¬ĘšŹ¼HClµÄĪļÖŹµÄĮæÅضČĪŖ____________mol/L.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖøʵĻī¶ÆŠŌ½éÓŚÄĘŗĶ¼ŲÖ®¼ä£ØøʵÄĆܶČĪŖ1.54æĖ/ĄåĆ×3£©£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A.ÉŁĮæµÄøĘ“¢“ęŌŚĆŗÓĶB.Ńõ»ÆŠŌ£ŗK+£¾Ca2+£¾Na+
C.øĘæÉŅŌ“ÓK2SO4ČÜŅŗÖŠÖĆ»»³ö¼ŲD.øĘÓėĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘŗĶŃõĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A.³£ĪĀĻĀ£¬ŌŚ0.1molL©1µÄHNO3ČÜŅŗÖŠ£¬ÓÉĖ®µēĄė³öµÄc£ØH+£©£¼ ![]()
B.ÅضČĪŖ0.1molL©1µÄNaHCO3ČÜŅŗ£ŗc£ØH2CO3£©£¾c£ØCO32©£©
C.25”ꏱ£¬AgCl¹ĢĢåŌŚµČĪļÖŹµÄĮæÅØ¶ČµÄNaCl”¢CaCl2ČÜŅŗÖŠµÄČܶȻżĻąĶ¬
D.±ł“×ĖįÖŠÖšµĪ¼ÓĖ®£¬ČÜŅŗµÄµ¼µēŠŌ”¢“×ĖįµÄµēĄė³Ģ¶Č”¢pH¾łĻČŌö“óŗó¼õŠ”
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com