
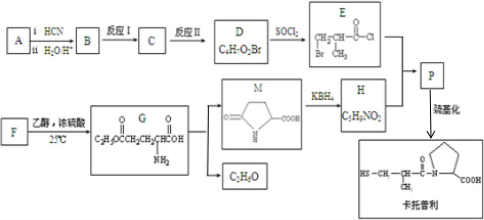
 (R1、R2为烃基)
(R1、R2为烃基)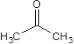 .
. ,反应Ⅱ所用试剂是HBr.
,反应Ⅱ所用试剂是HBr. .
.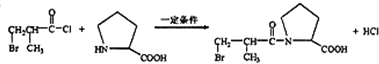 .
. (任写一种).
(任写一种).分析 D具有酸性,结合D的分子式可知,D含有羧基,由E的结构简式可知D为BrCH2CH(CH3)COOH,结合由给予的信息可知,A为 ,B为
,B为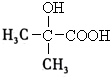 ,B发生消去反应生成C为CH2=C(CH3)COOH,C与HBr发生加成反应生成D.由卡托普利的结构可知,H为
,B发生消去反应生成C为CH2=C(CH3)COOH,C与HBr发生加成反应生成D.由卡托普利的结构可知,H为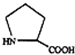 、P为
、P为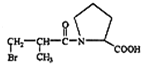 .由G的结构可知F为HOOCCH2CH2CH(NH2)COOH,G发生分子内酯交换得到M与乙醇,M发生还原反应得到H.
.由G的结构可知F为HOOCCH2CH2CH(NH2)COOH,G发生分子内酯交换得到M与乙醇,M发生还原反应得到H.
解答 解:D具有酸性,结合D的分子式可知,D含有羧基,由E的结构简式可知D为BrCH2CH(CH3)COOH,结合由给予的信息可知,A为 ,B为
,B为 ,B发生消去反应生成C为CH2=C(CH3)COOH,C与HBr发生加成反应生成D.由卡托普利的结构可知,H为
,B发生消去反应生成C为CH2=C(CH3)COOH,C与HBr发生加成反应生成D.由卡托普利的结构可知,H为 、P为
、P为 .由G的结构可知F为HOOCCH2CH2CH(NH2)COOH,G发生分子内酯交换得到M与乙醇,M发生还原反应得到H.
.由G的结构可知F为HOOCCH2CH2CH(NH2)COOH,G发生分子内酯交换得到M与乙醇,M发生还原反应得到H.
(1)D具有酸性,结合D的分子式可知,D含有羧基,故答案为:羧基;
(2)A的结构简式是: ,故答案为:
,故答案为: ;
;
(3)反应Ⅰ的化学反应方程式是: ,反应Ⅱ是CH2=C(CH3)COOH,HBr发生加成反应生成D,
,反应Ⅱ是CH2=C(CH3)COOH,HBr发生加成反应生成D,
故答案为: ;HBr;
;HBr;
(4)F为HOOCCH2CH2CH(NH2)COOH,在一定条件下可发生自身成肽反应,生成可降解的生物高分子,其中一种高分子物质的结构简式为: ,
,
故答案为: ;
;
(5)G→M的反应类型为取代反应,
故答案为:取代反应;
(6)E与H在一定条件下生成P的化学方程式是: ,
,
故答案为: ;
;
(7)H( )的同分异构体满足:①顺式结构、②具有两性、③含有甲基,符合条件的同分异构体为:
)的同分异构体满足:①顺式结构、②具有两性、③含有甲基,符合条件的同分异构体为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,明确有机物的官能团及其性质是解本题关键,充分利用有机物的性质与结构进行分析解答,需要学生对给予的信息进行利用,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | Q |
| A. | Y 的非金属性比Q强,所以HnY的酸性比HnQ强 | |
| B. | ZX2、WX2的熔沸点、硬度相差很大,这是由于它们的化学键类型不同造成的 | |
| C. | W、Q、Y 元素的原子半径及其简单离子半径依次减小 | |
| D. | 将足量的 X 单质通入 W 的氢化物的水溶液,能得到 W 的低价氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:H2O>NH3 | B. | 碱性:NaOH>Al(OH)3 | ||
| C. | 氧化性:F2>Cl2 | D. | 酸性:CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )| A. | 该电池可实现把化学能全部转化为电能 | |
| B. | 电极b上发生的电极反应为:02+2H2O+4e-=40H- | |
| C. | 电极a上发生的电极反应为:2H2S-4e-=S2+4H+ | |
| D. | 标况下,当有22.4LH2S参与反应时,有2mo1H+经质子膜进入负极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:MnO2>SO42->IO3->I2 | |
| B. | I2在反应①中是还原产物,在反应②中是氧化产物 | |
| C. | 反应①②中生成等量的I2时转移电子数之比为1:5 | |
| D. | NaHSO3溶液呈酸性,NaHSO3溶液中c(HSO3-)>c(H2SO3)>c(SO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1 mol•L-1NaHC2O4溶液(pH=5.5):c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| B. | 0.1 mol•L-1NaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | 0.1 mol•L-1 NH4HSO4溶液中滴加0.1 mol•L-1 NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1 mol•L-1CH3COOH溶液和0.1 mol•L-1CH3COONa溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其逆过程在相同条件下也必定是自发的 | |
| B. | 其逆过程在相同条件下也可能是自发的 | |
| C. | 其逆过程在其他条件下也可能是自发的 | |
| D. | 自发过程与外界条件无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com