
【题目】碳酸盐是重要的化工原料及试剂.
(1)向0.02mol/L Na2CO3溶液中加入等体积的CaCl2溶液若开始有沉淀生成,则所需CaCl2溶液的浓度最小为
(已知25℃时KSP(CaCO3)=2.8×10﹣9).通过最新工艺可制得纳米(50nm)CaCO3粉末,设计简
单的实验方法证明该物质的产生 .
(2)已知0.1mol/L NaHCO3溶液的pH=8.某学习兴趣小组探究实验室制得的纯碱含少量NaCl,还可能含少量NaHCO3 . 为测定纯碱的纯度,用电子天平准确称取样品m克,将其放入锥形瓶中,用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅色变成无色,且半分钟不变色,滴定过程中无气体产生,所用盐酸的体积为V1mL.
①用离子方程式便是此时发生的反应 .
②样品中Na2CO3质量分数的表达式是 .
③向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL.滴定终点时,溶液颜色的变化是 , 且半分钟内不变色;若样品中含 NaHCO3 , 则V1V2(填“>”、“<”或“=”).
【答案】
(1)5.6×10﹣7mol?L﹣1;取少量产品溶于水形成胶体,然后用一束可见光照射,侧面形成一条光亮通路
(2)CO32﹣+H+=HCO3﹣;![]() ×100%;溶液由黄色变为橙色;<
×100%;溶液由黄色变为橙色;<
【解析】解:(1)Na2CO3溶液的浓度为0.02mol/L,等体积混合后溶液中c(CO32﹣)= ![]() ×0.02mol/L=0.01mol/L,根据Ksp=c(CO32﹣)c(Ca2+)=2.8×10﹣9可知,c(Ca2+)=2.8×10﹣7mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10﹣7mol/L=5.6×10﹣7mol/L;
×0.02mol/L=0.01mol/L,根据Ksp=c(CO32﹣)c(Ca2+)=2.8×10﹣9可知,c(Ca2+)=2.8×10﹣7mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10﹣7mol/L=5.6×10﹣7mol/L;
因为纳米(50nm)CaCO3粉末,所以溶于水即形成胶体,则证明该物质的产生的方法为:取少量产品溶于水形成胶体,然后用一束可见光照射,侧面形成一条光亮通路;
所以答案是:5.6×10﹣7molL﹣1;取少量产品溶于水形成胶体,然后用一束可见光照射,侧面形成一条光亮通路;(2)①加酚酞指示剂,滴定至溶液由浅色变成无色,则变色范围在碱性,所以仅发生反应CO32﹣+H+=HCO3﹣;所以答案是:CO32﹣+H+=HCO3﹣;
②酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由浅色变成无色,指示CO32﹣+H+=HCO3﹣反应的终点,所用HCl溶液体积为V1mL,碳酸氢钠的质量为c×V1×10﹣3×M(Na2CO3)g,碳酸钠的质量分数为 ![]() ×100%=
×100%= ![]() ×100%,所以答案是:
×100%,所以答案是: ![]() ×100%;
×100%;
③用甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,指示HCO3﹣+H+=CO2+H2O反应的终点,所用HCl溶液体积为V2 mL,若V2=V1 , 只有Na2CO3;若V2>V1 , 则含有NaHCO3 , 所以答案是:溶液由黄色变为橙色;<.
【考点精析】通过灵活运用酸碱中和滴定,掌握中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点即可以解答此题.


科目:高中化学 来源: 题型:
【题目】(1)CH![]() 、CH3、CH
、CH3、CH![]() 都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH
都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH![]() 中四个原子是共平面的,三个键角相等,则键角应是________。
中四个原子是共平面的,三个键角相等,则键角应是________。
(2)叠氮化合物在化学工业上有重要应用。N![]() 叫做叠氮离子,请写出3种由三个原子构成的含有与N
叫做叠氮离子,请写出3种由三个原子构成的含有与N![]() 的电子数相同的粒子的化学式__________、__________、__________。
的电子数相同的粒子的化学式__________、__________、__________。
(3)N≡N键的键能为946 kJ/mol,N—N键的键能为193 kJ/mol,说明N2中的________键比________键稳定(填“σ”或“π”)
(4)CaC2中C![]() 与O
与O![]() 互为等电子体,O
互为等电子体,O![]() 的电子式可表示为________________;1 mol O
的电子式可表示为________________;1 mol O![]() 中含有的π键数目为________。
中含有的π键数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2molL﹣1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度所示,下列说法正确的是( ) 
A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH﹣ , Z表示H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置设计正确、且能达到目的是( ) 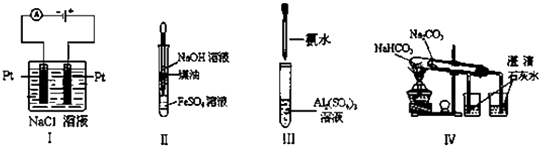
A.实验Ⅰ:制备金属钠
B.实验Ⅱ:制取氢氧化亚铁并观察其颜色
C.实验Ⅲ:制取少量的氢氧化铝
D.实验Ⅳ:比较两种物质的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A只由C、H、O三种元素组成,常用作有机合成的中间体,测得16.8 g该有机物完全燃烧生成44.0 g CO2和14.4 g水。质谱图表明其相对分子质量为84;红外光谱分析表明A中含有—O—H和位于分子端的C![]() CH,核磁共振氢谱显示有3种峰,且峰面积之比为6∶1∶1。
CH,核磁共振氢谱显示有3种峰,且峰面积之比为6∶1∶1。
(1)写出A的分子式____________;
(2)写出A的结构简式____________;
(3)下列物质一定能与A发生反应的是____________(填序号)
a.H2 b.Na
c.KMnO4 d.Br2
(4)有机物B是A的同分异构体,1 mol B可以与1 mol Br2加成,该有机物的所有碳原子在同一平面上,且没有顺反异构现象,则B的结构简式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的决定因素是( )
A.元素原子半径大小呈周期性变化B.元素的最高正化合价呈周期性变化
C.元素原子最外层电子排布呈周期性变化D.元素原子量依次递增
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应A(g)+3B(g)2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是( )
A.υ(A)=0.5mol/(Lmin)
B.υ(B)=0.12mol/(Ls)
C.υ(C)=0.1mol/(Ls)
D.υ(D)=0.4mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气的描述中,正确的是
A. 氯气的液态形式可称为氯水或液氯
B. 红热的铜丝在氯气中燃烧,生成蓝色氯化铜固体
C. 有氯气参加的反应必须在溶液中进行
D. 钠在氯气中燃烧,产生白烟
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com