
A、B、C、X、Y、Z元素的原子序数依次增大,根据信息完成问题:
|
元素A |
各能级上的电子数相等 |
|
元素C |
某种核素原子的质量数为18,中子数为10 |
|
元素X |
单质是良好的半导体材料 |
|
元素Y |
其单质为淡黄色晶体,常用来处理打碎的水银温度计 |
|
元素Z |
3d能级上有4个未成对电子 |
(1)Z元素在周期表中的位置 ,其电子排布式 。
(2)AO2的熔点远低于XO2熔点的主要原因是 。
(3)X的氧化物和NaOH溶液反应的化学方程式 。
(4)B、C气态基态原子的第一电离能的大小关系为 。
(5)请用离子方程式表达Na2Y溶液呈碱性的原因 。
(6)已知CH3COOH(aq)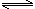 H+(aq)+CH3COO—(aq)
△H=+akJ/mol
H+(aq)+CH3COO—(aq)
△H=+akJ/mol
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) △H=—bkJ/mol
则中和热的△H= kJ/mol
(1)第四周期第Ⅷ族 (2分) 1s22s22p63s23p63d64s2 或[Ar]3d64s2 (2分)
(2)SiO2形成的是原子晶体,CO2形成的是分子晶体(2分)
(3)SiO2+2NaOH=Na2SiO3+H2O (2分)(4)N>O (2分)
(5)S2—+H2O HS—+OH— HS—+H2O
HS—+OH— HS—+H2O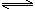 H2S+OH— (2分)
H2S+OH— (2分)
(6)—(a+b) (2分)
【解析】
试题分析:根据各能级上的电子数相等可推出A为C元素;根据某种核素原子的质量数为18,中子数为10可推出质子数为8,则C为O元素;根据原子序数依次增大可推出B为N元素;元素X的单质是良好的半导体材料,说明X为Si元素;元素Y的单质为淡黄色晶体,常用来处理打碎的水银温度计,说明Y为S元素;3d能级上有4个未成对电子,则Z为Fe。
(1)Z元素为Fe,在元素周期表中位于第四周期 Ⅷ族;电子排布式为:1s22s22p63s23p63d64s2 。
(2)CO2形成分子晶体,分子间以分子间作用力结合,SiO2是原子晶体,原子间以共价键结合,共价键作用远远大于分子间作用力,所以CO2的沸点远低于SiO2的沸点。
(3)SiO2为酸性氧化物,与NaOH反应生成Na2SiO3和H2O:SiO2+2NaOH=Na2SiO3+H2O
(4)N原子2P轨道排布3个电子,为半充满状态,为较稳定状态,失电子较难,所以第一电离能:N>O
(5)S2‾水解使溶液显碱性:S2—+H2O HS—+OH— HS—+H2O
HS—+OH— HS—+H2O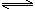 H2S+OH—
H2S+OH—
((6)中和热为反应:H++OH‾=H2O的∆H,根据盖斯定律,∆H=-∆H1+∆H2=—(a+b)kJ•mol‾1 。
考点:本题考查元素的推断、电子排布、沸点的比较、方程式的书写、盖斯定律的应用。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
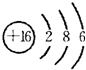

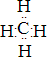
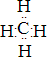
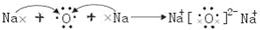
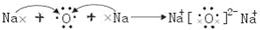
 2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是
2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中σ键与π键数目比为1:2 | 阳离子就是一个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
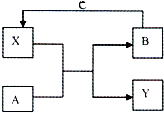 A、B、C、X和Y均为中学常见物质,其中A、B为单质,X、Y为化合物,C为地壳中含量最多的元素形成的单质,它们在一定条件下可发生如右图所示反应,请填空:
A、B、C、X和Y均为中学常见物质,其中A、B为单质,X、Y为化合物,C为地壳中含量最多的元素形成的单质,它们在一定条件下可发生如右图所示反应,请填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com