
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
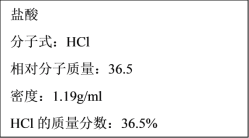
(1)该浓盐酸的物质的量浓度为___mol·L-1。
(2)某学生欲用上述浓盐酸和蒸馏水配制500ml物质的量浓度为0.4mol·L-1的稀盐酸,该学生需用量筒量取___ml上述浓盐酸进行配制。
(3)实验室用盐酸的浓溶液与高锰酸钾发生反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,该反应中的氧化剂是___,还原剂是___。(填化学式)
【答案】11.9 16.8 KMnO4 HCl
【解析】
(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度c= ![]() ;
;
(2)配制450mL物质的量浓度为0.4molL-1的稀盐酸,设需要浓盐酸体积为V,则依据溶液稀释规律,V×11.9mol/L=0.4mol/L×500mL,解得V;
(3)2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素化合价降低,是氧化剂;Cl元素化合价升高,是还原剂。
(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度c= ![]() =
= ![]() mol/L=11.9mol/L;故答案为:11.9;
mol/L=11.9mol/L;故答案为:11.9;
(2)配制450mL物质的量浓度为0.4molL-1的稀盐酸,由于实验室没有450mL的容量瓶,所以需要选择500mL的容量瓶,配制成500mL溶液,设需要浓盐酸体积为V,则依据溶液稀释规律,V×11.9mol/L=0.4mol/L×500mL,解得V=16.8mL;
(3)2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素化合价降低,是氧化剂;Cl元素化合价升高,是还原剂;故答案为:KMnO4;HCl。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】通过膜电池可除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是
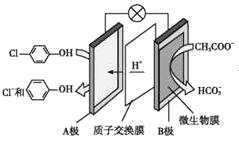
A.该方法能够提供电能
B.B极上的电势比A极上的电势低
C.A极的电极反应为![]() +H++2e-→Cl-+
+H++2e-→Cl-+![]()
D.电池工作时H+通过质子交换膜由正极区向负极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是
A. 强酸性溶液中:H+、NO3-、SO32-
B. pH=12的溶液中:OH-、K+、Cl-、HCO3-
C. 加入铝粉能放出氢气的溶液中一定存在:NH4+、NO3-、AlO2-、SO42-
D. 25C时pH=7的无色溶液中:Na+、Cl-、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
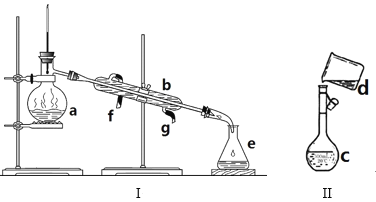
(1)写出下列仪器的名称:a、_____b、 _____
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是____,将仪器补充完整后进行实验,温度计水银球的位置在____处。冷凝水由____(填f或g)口通入,___口流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四位同学分别对四种溶液中所含的离子进行检测,结果如下,其中错误的是
A.Ca2+HCO3-Cl-K+B.OH-CO32-Cl-K+
C.Ba2+Na+OH-NO3-D.Cu2+ NO3-OH-Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:KClO3+HCl(浓)―KCl+ClO2↑+Cl2↑+
(1)请完成该化学方程式(将配平后的完整化学方程式写在答题卡上)。___
(2)浓盐酸在反应中显示出来的性质是___(填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生7.1gCl2,则生成ClO2的质量为___g。
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是Cl2的___倍(小数点后保留两位数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据了解,铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。
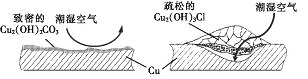
下列说法正确的是
A. Cu2(OH)3Cl属于有害锈
B. Cu2(OH)2CO3属于复盐
C. 青铜器表面刷一层食盐水可以做保护层
D. 用NaOH溶液法除锈可以保护青铜器的艺术价值,做到“修旧如旧”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可以得到粗盐,粗盐除还有NaCl外,还含有MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,各步操作流程如下。下列说法正确的是

A. 实验过程中①、⑤步骤的操作分别是溶解、过滤
B. 实验过程中步骤④的目的是仅除去溶液中的Ca2+
C. 实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、铁架台(带铁圈)
D. 实验过程中②、④步骤互换,对实验结果不影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曾在南充求学和工作过的青年学者孙旭平及其领衔团队,近日成功利用Mo2N纳米催化剂在0.1mol·L1盐酸溶液中进行电催化固氮,装置如图所示,在一定电压下具有较高的产氨速率。下列判断错误的是

A. Mo2N/GCE电极为阴极
B. 溶液中H+通过隔膜向MoN/GCE电极区迁移
C. Mo2N/GCE电极区反应式为N2+6H++6e====2NH3
D. 为提高溶液的导电性,可在石墨电极区加入适量的盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com