
下列说法不正确的是
A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除
B.常温下pH都等于5的CH3COOH溶液和NH4Cl溶液中,水的电离程度前者比后者大
C.BaSO4(s)+4C(s)===BaS(s)+4CO(g)室温下不能自发进行,说明该反应的ΔH﹤0
D.0.1 mol·L-1CH3COOH溶液加水稀释后,c(OH-)、CH3COOH的电离程度均增大
BC
【解析】
试题分析:因为CaCO3 的溶度积小于CaSO4 的溶度积,容易发生沉淀的转化CaSO4(s)+Na2CO3 = CaCO3 (s)+Na2SO4 ,生成了易溶于酸的CaCO3 ,可利用此反应除去水垢中的CaSO4 ,A项正确;醋酸是酸,酸抑制水的电离,NH4Cl属于能水解的盐,促进水的电离,所以pH都等于5的CH3COOH溶液和NH4Cl溶液中,水的电离程度前者比后者小,B项错误;根据△G=△H-T·△S可知,由于该反应是熵值增加的反应,室温下不能自发进行,说明反应应该是吸热反应,C项错误;CH3COOH溶液加水稀释,平衡正向移动,醋酸的电离程度增大,酸性减弱,碱性增强,D项正确;选BC。
考点:考查沉淀的转化,溶液中的平衡等知识。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2014-2015四川省攀枝花市高二上学期期末考试化学试卷(解析版) 题型:选择题
在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,有反应: CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol测得n(N2)随时间变化数据如下表:
温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(N2) | 0 | 0.20 | 0.25 | 0.40 | 0.40 |
T2 | n(N2) | 0 | 0.25 | …… | 0.30 | 0.30 |
下列说法不正确的是
A.0~10 min内,T1时V(N2)的平均反应速率比T2时的平均反应速率小
B.T1<T2
C.a < 0
D.在温度为T2时,向平衡后的容器中再充入1.2mol CH4,重新达平衡时n(N2)=0.40mol
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省吉安市高一上学期期末考试化学试卷(解析版) 题型:实验题
(11分)科学探究结果的准确性有赖于探究方法的科学性。某课外活动小组用下图装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。
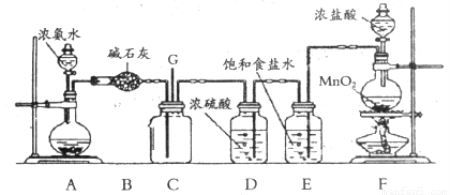
请回答下列问题:
(1)装置F中发生反应的化学方程式为_____________;浓盐酸在该反应中所表现出的性质为_____________、_____________。
(2)装置E的作用是:__________________________。
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式__________________________。
(4)该活动小组中甲、乙两位同学按下图装置继续进行实验:
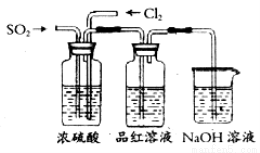
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是:__________________________,其有关反应的离子方程式为__________________________。
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?_______________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省吉安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列操作中,溶液的颜色不发生变化的是
A.氧化镁固体加入稀盐酸中,完全溶解
B.氢氧化铜加入到稀硫酸中
C.氯化铁溶液中加入足量铜粉,充分振荡
D.氯化铁溶液中滴加硫氰化钾(KSCN)溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:填空题
(10分)滴定实验是化学学科中重要的定量实验。请回答下列问题:
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250 mL溶液; ②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
滴定序号 | 待测液体积 | 所消耗盐酸标准的体积(mL) | |
滴定前 | 滴定后 | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
(1)用_____滴定管(填“酸式”或“碱式”)盛装0.10mol/L的盐酸标准液。
(2)试样中NaOH的质量分数为______________________。
(3)若出现下列情况,测定结果偏高的是___________。
a.滴定前用蒸馏水冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗
Ⅱ.氧化还原滴定—取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
(4)滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时滴定现象是________________。
Ⅲ.沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
(5)参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
D.纯碱溶于热水中去污效果增强,说明纯碱的水解是放热反应
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省泰州市姜堰区高一上学期期末化学试卷(解析版) 题型:填空题
(14分)结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的正确装置是 (填字母)。

将Cl2通入水中,所得溶液中具有氧化性的含氯粒子有 。
(2)氯气可用于生产漂白粉。由于盐酸浓度不同,漂白粉与盐酸混合发生反应的反应类型不同。
漂白粉与稀盐酸发生复分解反应,离子方程式为 。
漂白粉与浓盐酸发生氧化还原反应,离子方程式为 。
(3)某实验小组向100mL FeI2溶液中逐渐通入Cl2,会依次发生如下反应:
a.Cl2+2I-=2Cl-+I2
b.Cl2+2Fe2+=2Cl-+2Fe3+
c.5Cl2+I2+6H2O=10Cl-+2IO3-+12H+
其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示。

请回答下列问题:
①当n(Cl2)=0.12mol时,不考虑水的电离及金属离子的水解,分析溶液中所含金属阳离子及其
物质的量 (写出计算过程,否则不得分)。
②当溶液中n(Cl-):n(IO3-)=8:1时,通入的Cl2在标准状况下的体积为 L(写出计算过程,否则不得分)。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省泰州市姜堰区高一上学期期末化学试卷(解析版) 题型:选择题
下列物质中不属于电解质的是
A.NaOH B.CH4 C.H2SO4 D.KNO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市四校高三3月联合考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.玛瑙的主要成分为硅酸盐 B.pH小于7的雨水属于酸雨
C.漂白粉的有效成分是次氯酸钙 D.工业上用电解熔融的氯化铝冶炼铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com