
分析 铝与NaOH溶液反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据V=nVm计算生成的氢气的体积.
解答 解:令27g铝粉与足量氢氧化钠溶液充分反应是的氢气的物质的量为xmol,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54g 3mol
27g xmol
所以$\frac{54g}{27g}=\frac{3}{x}$,
解得x=1.5mol
标准状况下生成氢气的体积为1.5mol×22.4L/mol=33.6L,
答:标准状况下生成氢气的体积为33.6L.
点评 本题考查根据方程式的计算,比较基础,注意掌握根据方程式计算方法,根据方程式计算若左右单位不一致时,注意左右单位相当,上下单位一致.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
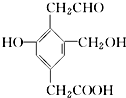 某有机物X的结构简式如图所示.若1mol X分别与H2、Na、NaOH、NaHCO3恰好完全反应,则消耗H2、Na、NaOH、NaHCO3的物质的量之比为( )
某有机物X的结构简式如图所示.若1mol X分别与H2、Na、NaOH、NaHCO3恰好完全反应,则消耗H2、Na、NaOH、NaHCO3的物质的量之比为( )| A. | 4:3:2:1 | B. | 3:3:2:1 | C. | 4:3:2:2 | D. | 3:3:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
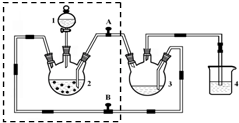
 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐的电离平衡被破坏 | B. | 水的电离程度一定会增大 | ||
| C. | 溶液的pH一定会增大 | D. | c(H+)与c(OH-)的乘积一定会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com