
(14分)铜及其化合物在生产生活中有广泛应用,铜在化合物中的常见化合价有+1、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。
(1)工业上可用Cu2S+O2 2Cu+SO2反应制取粗铜,该反应中是 元素被还原 。
2Cu+SO2反应制取粗铜,该反应中是 元素被还原 。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为: 温度控制在50℃-60℃的原因除了加快反应速率外,还有 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式 。
(3)现向Cu、Cu2O和CuO组成的混合物中,加入2 L 0.6 mol·L-1 HNO3溶液恰好使混合物溶解,同时收集到4480 mL NO气体(标准状况)。Cu2O跟稀硝酸反应的离子方程式 。若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。若混合物中含0.2 mol Cu,将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为 mol。
(14分)(1)Cu、O(2分);
(2)Cu+H2O2+2H+=Cu2++2H2O;(2分);防止H2O2分解(2分);
2Cu2++2Cl-+SO32-+H2O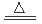 2CuCl↓+ SO42-+2H+(2分);
2CuCl↓+ SO42-+2H+(2分);
(3)3Cu2O+2NO3-+14H+=6Cu2++2NO↑+7H2O(2分);32(2分);0.2(2分).
【解析】
试题分析:(1)工业上可用Cu2S+O2 2Cu+SO2反应制取粗铜,在该反应中Cu、O元素的化合价降低,得到电子,被还原 ;(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为Cu+H2O2+2H+=Cu2++2H2O;温度控制在50℃-60℃的原因除了加快反应速率外,还有H2O2不稳定,温度高容易发生分解反应,在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式是2Cu2++2Cl- +SO32-+H2O
2Cu+SO2反应制取粗铜,在该反应中Cu、O元素的化合价降低,得到电子,被还原 ;(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为Cu+H2O2+2H+=Cu2++2H2O;温度控制在50℃-60℃的原因除了加快反应速率外,还有H2O2不稳定,温度高容易发生分解反应,在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式是2Cu2++2Cl- +SO32-+H2O 2CuCl↓+ SO42-+2H+;(3)Cu2O跟稀硝酸反应的离子方程式是3Cu2O+2NO3- +14H+= 6Cu2++2NO↑+7H2O;硝酸发生反应后得到的产物是Cu(NO3)2和NO,2 L ×0.6 mol/L=n(Cu(NO3)2)+ 4.480 L÷22.4L/mol,解得n(Cu(NO3)2)=1mol,根据原子守恒可得n(Cu2+)=0.5mol,所以若将上述混合物用足量的H2加热还原,所得到固体的质量为0.5mol×64g/mol=32g;若混合物中含0.2 mol Cu,则根据原子守恒可得:2n(Cu2O)+ n(CuO)=0.3mol;根据电子守恒可得:2n(Cu)+ 2n(Cu2O)= 3×(4.480 L÷22.4L/mol).解得n(CuO)= 0.1mol;n(Cu2O)=0.1mol,Cu与硫酸不反应,CuO和Cu2O与硫酸反应的方程式是:CuO+H2SO4=CuSO4+H2O, Cu2O+H2SO4=CuSO4+Cu+H2O,则根据物质反应时的物质的量关系可知将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为0.1mol+0.1mol=0.2mol。
2CuCl↓+ SO42-+2H+;(3)Cu2O跟稀硝酸反应的离子方程式是3Cu2O+2NO3- +14H+= 6Cu2++2NO↑+7H2O;硝酸发生反应后得到的产物是Cu(NO3)2和NO,2 L ×0.6 mol/L=n(Cu(NO3)2)+ 4.480 L÷22.4L/mol,解得n(Cu(NO3)2)=1mol,根据原子守恒可得n(Cu2+)=0.5mol,所以若将上述混合物用足量的H2加热还原,所得到固体的质量为0.5mol×64g/mol=32g;若混合物中含0.2 mol Cu,则根据原子守恒可得:2n(Cu2O)+ n(CuO)=0.3mol;根据电子守恒可得:2n(Cu)+ 2n(Cu2O)= 3×(4.480 L÷22.4L/mol).解得n(CuO)= 0.1mol;n(Cu2O)=0.1mol,Cu与硫酸不反应,CuO和Cu2O与硫酸反应的方程式是:CuO+H2SO4=CuSO4+H2O, Cu2O+H2SO4=CuSO4+Cu+H2O,则根据物质反应时的物质的量关系可知将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为0.1mol+0.1mol=0.2mol。
考点:考查有关铜元素的单质及化合物的转化、性质、计算的知识。


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:实验题
(10分)某氯化铁样品含有FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
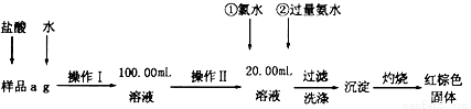
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 (填仪器名称).
(2)加入过量氨水生成沉淀的离子方程式为 ;
(3)若不用氯水,可用下列试剂中的 代替(填序号)。
A.H2O2 B.碘水 C.NaClO
(4)步骤⑤中检验沉淀是否洗净的方法是 。
(5)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为 (请把结果约到最简)。
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列有关实验的做法错误的是( )
A.分液时,分液漏斗中的上层液体应由上口倒出
B.用加热的方法可区分碳酸钠和碳酸氢钠两种固体
C.用渗析的方法可除去Fe(OH)3胶体中混有的Cl-
D.加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列解释事实的离子方程式不正确的是
A.84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+=Cl2↑+H2O
B.向水玻璃中加入盐酸有白色沉淀生成:2H++SiO32-=H2SiO3↓
C.SO2使紫色石蕊溶液变红色:SO2+H2O  2H++SO32-
2H++SO32-
D.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HClO
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关物质性质的说法错误的是
A.热稳定性:HCl>HBr>HI
B.原子半径:Na>Mg>Al
C.还原性:PH3>H2S>HCl
D.结合质子能力:ClO->HCO3->SiO32-
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列实验能达到相应目的的是
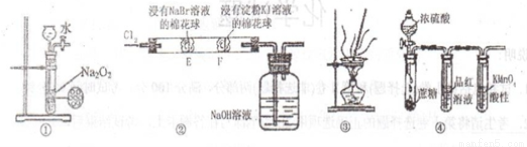
A.用图①装置制备少量的氧气
B.用图②可证明氧化性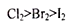
C.用图③装置将海带灼烧成灰
D.用图④装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子或分子在指定分散系中一定能大量共存的是
A.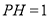 的溶液中:
的溶液中: 、
、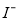 、
、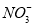 、
、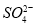
B.氢氧化铁胶体中: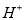 、
、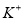 、
、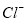 、
、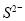
C.在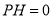 的溶液中:
的溶液中: 、
、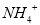 、
、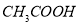 、
、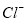
D.水电离产生的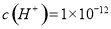
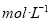 的溶液中HCO3-、
的溶液中HCO3-、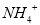 、
、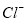 、
、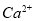
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市诸城高三10月月考化学试卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是
A.NH3通人AlCl3溶液中
B.用脱脂棉包裹Na2O2粉末露置在潮湿空气中
C.CO2通入CaCl2溶液中
D.稀盐酸滴加到Fe(OH) 3胶体溶液中
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高三10月阶段测试化学试卷(解析版) 题型:选择题
用下面的方案进行某些离子的检验,其中方案设计得最严密的是( )
A.检验试液中的SO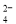 :试液
:试液 无沉淀
无沉淀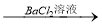 白色沉淀
白色沉淀
B.检验试液中的Fe2+:试液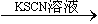 无明显现象
无明显现象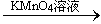 红色溶液
红色溶液
C.检验试液中的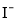 :试液
:试液 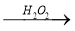 棕黄色溶液
棕黄色溶液 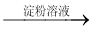 蓝色溶液
蓝色溶液
D.检验试液中的CO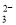 :试液
:试液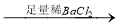 白色沉淀
白色沉淀 沉淀溶解
沉淀溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com