
一定条件下,在一密闭容器中将1.0 mol/L N2与3.0 mol/L H2合成氨,反应到2s时测得
NH3的浓度为0.8 mol/L,用N2浓度的变化量来表示该反应速率时,该反应的反应速率为
A、0.2 mol/(L·s) B、0.4 mol/(L·s) C、0.6 mol/(L·s) D、0.8 mol/(L·s)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。据此,判断五种金属的活动性顺序是( )
A.A>B>C>D>E B.A>C>D>B>E
C.C>A>B>D>E D.B>D>C>A>E
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列有关叙述正确的是
A.标准状况下,44.8L苯中分子数为2NA
B.1mol水中含氢离子数为NA
C.5.6g铁与足量稀硫酸完全反应失去电子数为0.3NA
D.16 g CH4与18 g NH4+ 所含电子数均为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
从A出发,发生图示中的系列反应,其中B分子核磁共振氢谱有三组峰,峰面积比为1:2:2,F的苯环上一氯代物只有一种,Z和G均不能与金属钠反应,且互为同分异构体。

回答下列问题:
(1)F的化学名称为 。
(2)反应④的化学方程式为 ,在①~⑦的反应中,属于取代反应的有 。
(3)B的结构简式为 ,其所含官能团名称为 。
(4)E和F反应生成G的化学方程式为 。
(5)与B互为同分异构体,属于酚类且苯环上只有对位两取代的化合物有 种,写出可能的结构简式 , , , ,。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关l3C、15N的下列说法正确的是
A.13C与15N有相同的中子数 B.13C与C60互为同素异形体
C. 15N与14N互为同位素 D.15N和14N的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关碱金属的说法正确的是
A、碱金属元素随原子序数的递增原子半径逐渐减小
B、碱金属元素随原子序数的递增离子氧化性逐渐减弱
C、碱金属元素的单质在氧气点燃都生成过氧化物
D、碱金属元素随原子序数的递增最高价氧化物对应的水化物碱性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)硫、碳、硅是三种重要的非金属元素,请回答下列问题:
(1)它们的非金属性由强到弱的顺序是 (用元素符号表示),
| |
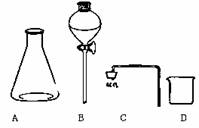
(2)请你用题中所给仪器设计一套装置证明(1)中的结论,在右边方框
中画出装置图;仪器B的名称是 。
(3)实验过程中在仪器B 中应装入的试剂是 ,烧杯中出现的现
象是 。若锥形瓶中装的是一种能溶于水的正盐,则
其中发生反应的离子方程式为 。
| |
(1)在右边方框中画出装置图。
(2)若实验时,M上有气泡,N上没气泡,则M的最高价氧化物对应
的水化物的碱性比N的最高价氧化物对应的水化物的碱性比
(填“强”或“弱”),外电路中电子由 (填M或N)极流
向 (填M或N)极。
查看答案和解析>>
科目:高中化学 来源: 题型:
向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
A.①中仅发生一个反应 B.Fe3+能催化H2O2的分解
C.反应过程中溶液pH不断减小 D.FeSO4与等物质的量的H2O2恰好反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com