
分析 (1)阴极、阳极都有气体产生,且体积比(相同条件下)为2:1,应为电解水的反应;
(2)阴极、阳极都有气体产生,且体积比(相同条件下)为1:1,题中应该为电解NaCl溶液,分别生成氯气和氢气;
(3)阴极、阳极都有气体产生,如溶液pH变小,则酸性增强,可为电解硫酸溶液,浓度增大,如pH变大,可为电解KOH溶液;
(4)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小,只有硫酸铜符合.
解答 解:(1)电解①②⑤时,阴极氢离子放电,生成氢气,即4H++4e-→2H2↑,阳极氢氧根离子放电,生成氧气,
即4OH--4e-=O2↑+2H2O,两极都有气体产生,且体积比(相同条件下)为2:1,
故答案为:①②⑤;
(2)阴极、阳极都有气体产生,且体积比(相同条件下)为1:1,题中应该为电解NaCl溶液,分别生成氯气和氢气,阳极反应为2Cl--2e-=Cl2↑,总方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2+Cl2,
故答案为:③;2Cl--2e-=Cl2↑;2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(3)阴极、阳极都有气体产生,如溶液pH变小,则酸性增强,可为电解硫酸溶液,浓度增大,如pH变大,可为电解KOH溶液,另外电解NaCl溶液,生成NaOH,pH也变大,故答案为:①;③⑤;
(4)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小,只有硫酸铜符合,电解的总方程式为2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4,
故答案为:④;2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4.
点评 本题考查电解知识,为高频考点,把握离子放电顺序为解答该题的关键,侧重分析与应用能力的考查,注意把握电极和电解方程式的书写,题目难度不大.


科目:高中化学 来源: 题型:实验题
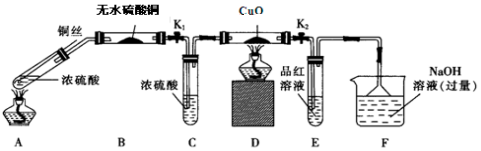
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a电极是该电池的负极,发生氧化反应 | |
| B. | b电极反应式为2NO3-+10e-+12H+═N2↑+6H2O | |
| C. | 电池工作时,H+由左室通过质子交换膜进入右室 | |
| D. | 转化室中发生反应后溶液的pH增大(忽略体积变化) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
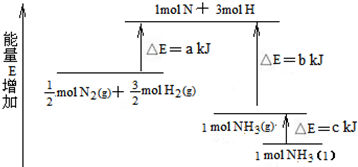
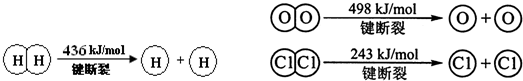
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管未用盐酸润洗就直接注入标准盐酸 | |
| B. | 滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 | |
| C. | 酸式滴定管在滴定前有气泡,滴定后气泡消失 | |
| D. | 读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物 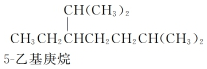 的名称为2,6二甲基5乙基庚烷 的名称为2,6二甲基5乙基庚烷 | |
| B. | 丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 | |
| C. | 化合物  是苯的同系物 是苯的同系物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
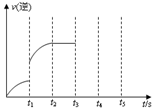 一定温度下在体积为5L的密闭容器中发生某可逆反应,其化学平衡常数表达式为:$K=\frac{{c(CO)•c({H_2})}}{{c({H_2}O)}}$
一定温度下在体积为5L的密闭容器中发生某可逆反应,其化学平衡常数表达式为:$K=\frac{{c(CO)•c({H_2})}}{{c({H_2}O)}}$查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C O (g)+O2(g)═2CO2(g) | B. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) | ||
| C. | 2H2(g)+O2(g)═2H2O(l) | D. | Zn(s)+Ag2 O(s)═Zn O(s)+2Ag(s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com