
【题目】在一定温度下的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
A.容器内的压强不再改变B.c(SO2):c(O2):c(SO3)=2:1:2
C.SO2的转化率不再改变D.SO3的生成速率与SO3的消耗速率相等
【答案】B
【解析】
根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态。
A.该反应为反应前后气体的总量发生变化的反应,容器内的压强不再改变时,说明气体的物质的量也不再发生变化,反应达平衡状态,故A正确;
B.c(SO2):c(O2):c(SO3)=2:1:2,只能说明某一时刻各物质的浓度之间的关系,不能说明各物质的物质的量浓度不变,故B错误;
C.SO2的转化率不再改变,说明各物质的量不变,反应达平衡状态,故C正确;
D.SO3的生成速率与SO3的消耗速率相等,说明正、逆反应的速率相等,反应达平衡状态,故D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。
请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为________,第一电离能最小的元素是________(填元素符号)。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是________(填化学式),呈现如此递变规律的原因是___________________。
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为________。另一种的晶胞如图二所示,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为________________________________________________g·cm-3(保留两位有效数字)。(![]() =1.732)
=1.732)

图一 图二 图三
(4)D元素形成的单质,其晶体的堆积模型为________,D的醋酸盐晶体局部结构如图三,该晶体中含有的化学键是________(填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(5)向D的硫酸盐溶液中滴加过量氨水,观察到的现象是________。请写出上述过程的离子方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为气相直接水合法C2H4(g)+H2O(g)![]() C2H5OH(g)中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
C2H5OH(g)中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]。
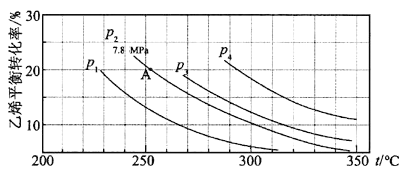
计算乙烯水合制乙醇反应在图中A点的平衡常数Kp为 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
A.0.082B.0.072C.0.072MPa-1D.0.082 MPa-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是___________;核外未成对电子数是___________个。
(2)该超分子中存在的化学键类型有___________。
A σ键 B π键 C 离子键 D 氢键
(3)该超分子中配体CO提供孤电子对的原子是___________(填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________。
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因___________。
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是___________。
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。

钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及(1/2,1/2,1/2)。根据以上信息,推断该晶体的原子堆积方式是___________。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是M g·mol-1,阿伏加德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为___________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol/L的NH4Cl溶液中,离子浓度关系正确的是
A.c(![]() )>c(Cl—)>c(H+)>c(OH—)
)>c(Cl—)>c(H+)>c(OH—)
B.c(![]() )>c(OH—)>c(Cl—)>c(H+)
)>c(OH—)>c(Cl—)>c(H+)
C.c(OH—)=c(Cl—)+c(H+)
D.c(![]() )+c(H+)=c(Cl—)+c(OH—)
)+c(H+)=c(Cl—)+c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石与石墨是同素异形体。100 kPa时,1 mol石墨转化为金刚石的能量变化如图所示,下列说法正确的是

A.石墨转化为金刚石的反应为放热反应
B.石墨比金刚石更稳定
C.金刚石比石墨更稳定
D.破坏1 mol石墨的化学键所吸收的能量小于形成1 mol金刚石的化学键所放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
A.将稀氨水逐滴加入稀硫酸中,当溶液的![]() 时,
时,![]()
B.两种醋酸溶液的物质的量浓度分别为![]() 和
和![]() ,pH分别为a和
,pH分别为a和![]() ,则
,则![]()
C.![]() 的NaOH溶液与
的NaOH溶液与![]() 的醋酸溶液等体积混合,滴入石蕊溶液呈红色
的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向![]() 的氨水中加入少量硫酸铵固体,则溶液中
的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可降解高分子化合物H的合成路线如下
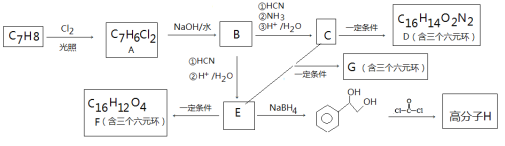
已知:i.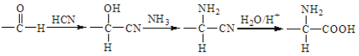
ii.![]() +2ROH
+2ROH ![]()
![]() +2HCl(R为烃基)
+2HCl(R为烃基)
回答下面问题:
(1)有机物C中含有官能团的名称________;
(2)有机物E生成F的反应类型_________;
(3)有机物D的结构简式_________,高分子化合物H的结构简式_________;
(4)具有相同官能团的有机物A的同分异构体有_________种;
(5)有机物E和C按1:1发生缩聚反应的化学方程式:__________;
(6)写出由乙烯合成多肽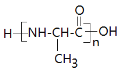 的合成路线图(其他无机试剂任选)____________。
的合成路线图(其他无机试剂任选)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法中,正确的是
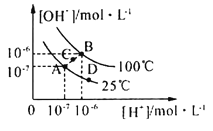
A.图中A、B、D三点处Kw的大小关系:B>A>D
B.25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3·H2O)的值逐渐减小
C.在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com