
| A. | 0.2mol•L-1醋酸溶液和0.2mol•L-1醋酸钠溶液等体积混合:C(CH3COOH)+C(H+)-C(OH-)=0.1mol•L-1 | |
| B. | pH相等的①(NH4)2SO4②NH4HSO4③NH4Cl溶液:c(NH4+)大小顺序为:①>②>③ | |
| C. | 0.1mol•L-1Na2CO3溶液中c(Na+)+c (H+)=C (CO32-)+c(HCO3-)+c(OH-) | |
| D. | 0.1mol•L-1的NaHB溶液,其中PH=4:c(HB-)>c(H+)>c(H2B)>c(B2-) |
分析 A.根据混合液中的电荷守恒和物料守恒分析;
B.硫酸氢铵溶液为强酸性溶液,其溶液中铵根离子浓度最小;硫酸铵和氯化铵溶液中都是铵根离子水解导致溶液显示酸性,两溶液中铵根离子浓度相等;
C.根据碳酸钠溶液中的电荷守恒判断;
D.0.1mol•L-1的NaHB溶液的pH=4,说明HB-的电离程度大于其水解程度,则c(B2-)>c(H2B).
解答 解:A.0.2mol•L-1醋酸溶液和0.2mol•L-1醋酸钠溶液等体积混合,由于醋酸的电离程度大于醋酸根离子的水解程度,则溶液显示酸性,根据电荷守恒可得:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),根据物料守恒可得:c(CH3COOH)+c(CH3COO-)=2c(Na+),二者结合可得:c(CH3COOH)+c(H+)-c(OH-)=c(Na+)=0.1mol•L-1,故A正确;
B.pH相等的①(NH4)2SO4②NH4HSO4③NH4Cl溶液,硫酸氢铵完全电离出氢离子,其溶液的浓度最小,则铵根离子浓度最小;硫酸铵和氯化铵溶液的pH相等,则铵根离子浓度相等,故三种溶液中c(NH4+)大小顺序为:①=③>②,故B错误;
C.0.1mol•L-1Na2CO3溶液中,根据电荷守恒可知:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故C错误;
D.0.1mol•L-1的NaHB溶液的pH=4,说明HB-的电离程度大于其水解程度,则c(B2-)>c(H2B),氢离子还来自水的电离,则溶液中正确的离子浓度大小为:c(HB-)>c(H+)>c(B2-)>c(H2B),故D错误;
故选A.
点评 本题考查了离子浓度大小比较、盐的水解原理及其应用,题目难度中等,注意掌握电荷守恒、物料守恒及盐的水解原理的应用,明确判断离子浓度大小常用方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2CO2=2Na2CO3+O2 | B. | Na2O+CO2=Na2CO3 | ||
| C. | 2NaOH+CO2=Na2CO3+H2O | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al原子的最外层电子数依次减少 | |
| B. | N、O、F元素的最高正价依次升高 | |
| C. | C、N、O的原子半径依次减小 | |
| D. | Li、Na、K的金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
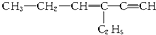 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,一定在同一平面上的碳原子数为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,一定在同一平面上的碳原子数为c,则a、b、c分别为( )| A. | 4,3,5 | B. | 4,3,6 | C. | 2,5,4 | D. | 4,6,4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
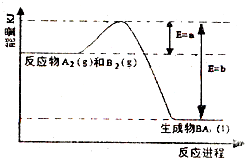 原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题:
原子序数依次增大的A、B、C、D、E五种短周期元素,A是原子半径最小的元素,B的单质分子中有三对共用电子,C最外层电子数是次外层电子数的3倍,A、D同主族,E原子电子数比C原子电子数多5个,请回答下列问题: ,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;
,以W溶液作为电解质溶液,E棒与铁棒分别作为电极构成原电池,则负极的电极反应式Al-3e-+4OH-=AlO2-+2H2O;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖 | |
| B. | 石油裂解和油脂皂化都是高分子生成小分子的过程 | |
| C. | 分子式为C2H4O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| D. | 乙醇、乙酸和乙醛能用新制Cu(OH)2悬浊液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
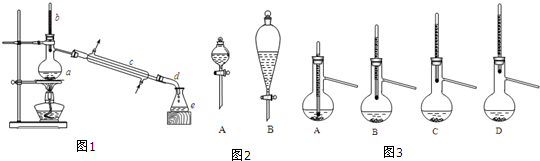
| 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 | |
| 密度/(g/cm3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 118.0 | 118.1 | 126.1 | 142 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al原子最外层电子数依次减少 | |
| B. | C、N、O元素非金属性依次增强 | |
| C. | C、N、O元素最高正价依次增大 | |
| D. | Li、Na、K的金属性依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com