
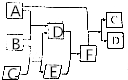
 有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:
有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:分析 常见由两种元素组成且均含10个电子物质有HF、OH-、H2O、NH2-、NH3、H3O+、CH4、NH4+等,其中B既能与A反应也能与C反应,由转化关系可知B应为OH-,A为H3O+,C为NH4+,则D为H2O,E为NH3,F为NH3•H2O,以此解答该题.
解答 解:常见由两种元素组成且均含10个电子物质有HF、OH-、H2O、NH2-、NH3、H3O+、CH4、NH4+等,其中B既能与A反应也能与C反应,由转化关系可知B应为OH-,A为H3O+,C为NH4+,则D为H2O,E为NH3,F为NH3•H2O,
(1)A为H3O+,含有3个δ键和1个孤电子对,则应为三角锥形,C为NH4+,含有4个δ键,没有孤电子对,为正四面体,故答案为:三角锥形;正四面体;
(2)等电子体是指具有原子总数相同、价电子总数相同的微粒,六种物质中H3O+、NH3互为等电子体,故答案为:H3O+、NH3;
(3)A~E五种微粒中含有配位键的有H3O+、NH4+,故答案为:H3O+、NH4+;
(4)将过量的F滴加到CuSO4溶液中,生成深蓝色的溶液,溶液中生成铜氨络离子,生成物为[Cu(NH3)4]SO4,故答案为:[Cu(NH3)4]SO4.
点评 本题考查无机物的推断,侧重于学生的分析能力的考查,为高考常见题型和高频考点,注意常见10电子和18电子物质的种类和性质,结合转化关系可判断出物质的种类,难度不大,学习中注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 在分子组成上相差一个或若干个CH2原子团的物质一定互称为同系物 | |
| B. | 具有同分异构现象的有机化合物互称为同分异构体 | |
| C. | 同素异形体是指同种元素形成不同的单质 | |
| D. | 含有相同的质子数而不同的中子数的同一类元素的原子互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
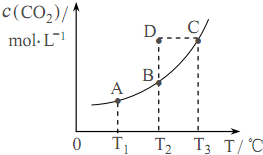 在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )
在密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( )| A. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| B. | 在T2时,若反应处于状态D,则一定有V正<V逆 | |
| C. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H<0 | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
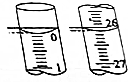 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
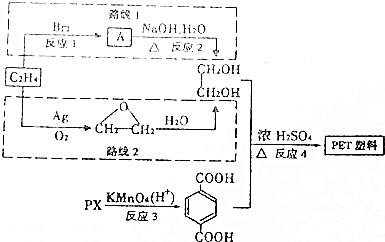

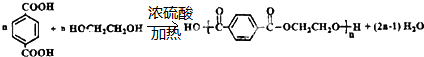 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水与盐酸恰好中和后的溶液:c(H+)>c(OH-) | |
| B. | 0.2mol/L醋酸溶液与0.1mol/L NaOH溶液等体积混合后的溶液:c(CH3COO-)+c(CH3COOH)=0.2mol/L | |
| C. | NaHSO3溶液(呈酸性):c(Na+)>c(HSO3-)>c(H+)>c(OH-) | |
| D. | NaHSO4溶液滴入氨水后的溶液:c(H+)+c(NH4+)=2c(SO42-)+c(OH-). |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第一次月考化学卷(解析版) 题型:选择题
下列分散系最不稳定的是
A.向NaOH溶液中通入CO2得到的无色溶液
B.向碘的水溶液中滴加四氯化碳充分振荡后,静置后的下层液体
C.向沸水中滴入饱和的FeCl3溶液得到的红褐色液体
D.向稀硫酸中加入BaCl2溶液得到的分散系
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上第一次月考化学卷(解析版) 题型:实验题
用碳酸钠晶体(Na2CO3•10H2O),配制0.2mol/L的Na2CO3溶液480mL。
(1)所需主要仪器为:药匙、托盘天平、烧杯、玻璃棒、_________和胶头滴管。
(2)本实验所需称量碳酸钠晶体(Na2CO3•10H2O)_________g;
(3)根据下列操作对所配溶液的浓度产生的影响,完成下列要求。
①Na2CO3•10H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有_________,偏低的有__________,无影响的有_________。(填序号)
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:

你认为该同学的操作步骤中错误(包含遗漏)之处有___________。
A.1处 | B.2处 | C.3处 | D.4处 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:选择题
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴以下危险警告标签。下面所列物质中,贴错了标签的是( )
| A | B | C | D |
|
物质的 | H2SO4(浓) | 乙醇 | KCl | KCN |
|
危险警告标签 |
|
|
|
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com