
| A. | 可溶于水 | B. | 熔融状态能导电 | C. | 水溶液能导电 | D. | 具有较高熔点 |
 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 不能用磁铁将Fe与Fe3O4分离 | |
| B. | 将生成的气体在空气中冷却可获得钠 | |
| C. | 该反应条件下铁的氧化性比钠强 | |
| D. | 该反应中每生成2 mol H2,转移的电子数约为4×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
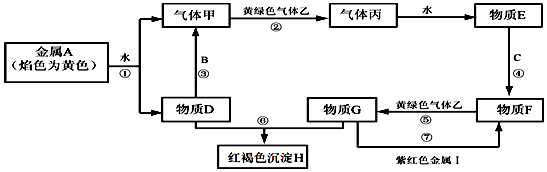
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
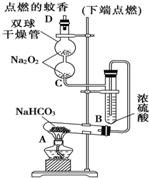 如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3,D为固定有燃着蚊香的硬纸片.试回答下列问题:
如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3,D为固定有燃着蚊香的硬纸片.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验现象 | 分析或结论 | |
| A | 光照新制氯水有气泡冒出 | 氯水含有Cl2,光照Cl2逸出 |
| B | 液氯滴到干燥的有色布条会褪色 | 液氯中的次氯酸具有漂白性 |
| C | 往NaHCO3固体加入新制氯水,有无色无味的气体产生 | 氯水中含有盐酸与NaHCO3反应,产生CO2 |
| D | 新制氯水放置数天后,pH值将增大 | 氯化氢具有挥发性,酸性减弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH试纸放入某溶液中,显色后和标准比色卡对比以测定该溶液的pH | |
| B. | 过滤操作时,漏斗下部的尖嘴要紧靠烧杯的内壁 | |
| C. | 某溶液加氯化钡溶液有白色沉淀生成,说明原溶液中一定有SO42- | |
| D. | 向溶液中先滴加氯水,再滴加KSCN溶液,溶液呈红色,说明原溶液中一定含Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com