
�Ͼ���ʾ�������к�SiO2��Fe2O3��CeO2��FeO�����ʡ�ij����С���Դ˲�����ĩΪԭ�ϣ��Ƶ�Ce(OH)4��������立���Fe2(SO4) 3��(NH4) 2SO4��24H2O�ݣ�����������£�

��֪�������������£�����ˮ��Һ����Ce3+��Ce4+������Ҫ������ʽ��Ce4+�н�ǿ�����ԣ���CeO2������ϡ���ᣬҲ������NaOH��Һ��
�ش��������⣺
(1)��Ӧ�ٵ����ӷ���ʽ�� ��
(2)��Ӧ����H2O2�������� ��
(3)��Ӧ�۵����ӷ���ʽ�� ��
(4)��֪�л���HT�ܽ�Ce3+��ˮ��Һ����ȡ�������ù��̿ɱ�ʾΪ��
2Ce3+ (ˮ��)+ 6HT(�л���) 2CeT3 (�л���)+ 6H+(ˮ��)
2CeT3 (�л���)+ 6H+(ˮ��)
��ƽ��ǶȽ��ͣ���CeT3 (�л���)����H2SO4 ��ýϴ��ĺ�Ce3+��ˮ��Һ��ԭ���� ��
(5)������立���Fe2(SO4) 3��(NH4) 2SO4��24H2O�ݹ㷺����ˮ�ľ����������侻ˮԭ�������ӷ���ʽ������ ��
 ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д� һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ���½���ѧ����У�����ϵ�һ��������ѧ���������棩 ���ͣ�ѡ����
��H2O2��Һ������NaCN�ķ�ˮ�ķ�Ӧԭ��ΪNaCN + H2O2 + H2O = NaHCO3 + NH3 ����֪��HCN�����Ա�H2CO3���������й�˵����ȷ����( )
A���÷�Ӧ�е�Ԫ�ر�����
B���÷�Ӧ��H2O2����ԭ��
C��0.1mol��L-1NaCN��Һ�к���HCN��CN-������Ϊ0.1��6.02��1023
D��ʵ��������NaCN��Һʱ�������������NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�Ͳ��и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��������������ء�����˵����ȷ����
A���ӵ��ε���Һ�����۱���
B�����ͺͲ��;�Ϊʯ�ͷ���õ��IJ�Ʒ
C��CaCO3��������ҵ�����������
D�����ǡ����ۡ�����������ˮ�����γɽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ��һ�ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��1mol�������������22.4L
B��1molH2 ��������1g������ռ�������22.4L
C���ڱ�״���£�1mol�κ�������ռ�������ԼΪ22.4L
D���ڱ�״���£�1mol�κ�������ռ�������ԼΪ22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ��һ�ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������˵������ȷ����
A��1 mol N2�����е�ԭ����ΪNA
B����״���£�22.4 Lˮ�к��е�ˮ������ΪNA
C����״���£�22.4 L�Ȼ���������ԭ����ΪNA
D��32 g O2��������ԭ����ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��㶫ʡɽһ������ѧ�ڵ�һ��ͳ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��3�ݵ�������С�մ�1�� ֱ��������ǡ����ȫ��Ӧ����2�����ȼ��ȣ�ʹ�䲿�ַֽ����������ǡ����ȫ��Ӧ����3�����ȼ��ȣ�ʹ����ȫ�ֽ����������ǡ����ȫ��Ӧ��������������ʵ���Ũ����ͬ���������������ֱ�ΪV1��V2��V3����V1��V2��V3�Ĵ�С��ϵ��ȷ����
ֱ��������ǡ����ȫ��Ӧ����2�����ȼ��ȣ�ʹ�䲿�ַֽ����������ǡ����ȫ��Ӧ����3�����ȼ��ȣ�ʹ����ȫ�ֽ����������ǡ����ȫ��Ӧ��������������ʵ���Ũ����ͬ���������������ֱ�ΪV1��V2��V3����V1��V2��V3�Ĵ�С��ϵ��ȷ����
A��V1>V2>V3 B��V1>V3>V2 C��V2>V3>V1 D��V1��V2��V3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��㶫ʡɽһ������ѧ�ڵ�һ��ͳ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A��5.6 g ������0.1mol�����г��ȼ�գ�ת�Ƶ�����Ϊ0.3NA
������0.1mol�����г��ȼ�գ�ת�Ƶ�����Ϊ0.3NA
B��2.5mL 16mol��L-1Ũ����������ͭ��Ӧ��ת�Ƶ�����Ϊ0.04NA
C��7.8g Na2S��Na2O2�Ĺ��������к��е�������������0.1NA
D�������£�5.6 g ����������Ũ���ᷴӦ��ת�Ƶĵ�����Ϊ0.3 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��״����VL�����ܽ���1Lˮ�У�������Һ���ܶ�Ϊ�� g/ml����������Ϊ�أ�����Ũ��Ϊc mol/L�������й�ϵ����ȷ���ǣ� ��
A��c =  B���� =
B���� = 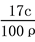
C���� = 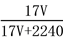 D���� =
D���� = 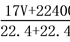
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶���9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪4NH3+5O2��4NO+6H2O ������Ӧ���ʷֱ���V(NH3)�� V(O2)��V(NO)��V(H2O)��ʾ������ȷ�Ĺ�ϵ�ǣ� ��
A�� V(NH3)=V(O2) B��
V(NH3)=V(O2) B��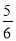 V(O2)=V(H2O)
V(O2)=V(H2O)
C��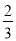 V(NH3)=V(H2O) D��
V(NH3)=V(H2O) D�� V(O2)=V(NO)
V(O2)=V(NO)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com