
| A. | 往某溶液中加入稀NaOH溶液,无刺激性气味的气体产生,说明该溶液一定不含NH4+ | |
| B. | 用加热的方法可以除去混在NaCl固体中的NH4Cl,说明NH4Cl会升华 | |
| C. | SO2气体和Cl2均能使品红溶液褪色,说明两者均有强氧化性 | |
| D. | 浓硫酸可用来干燥H2、Cl2、SO2等气体,说明浓硫酸具有吸水性 |
分析 A.铵盐的稀溶液中加入氢氧化钠溶液反应生成一水合氨,加热会生成氨气;
B.氯化铵受热分解生成氯化氢和氨气,上升过程中相遇会生成固体氯化铵,升华是物质三态变化属于物理变化;
C.二氧化硫与有色物质发生化合反应生成无色物质,没有发生氧化还原反应;
D.浓硫酸具有吸水性,能作干燥剂.
解答 解:A.铵盐的稀溶液中加入氢氧化钠溶液反应生成一水合氨,无刺激性气味的气体产生,加热会分解生成氨气,故A错误;
B.用加热的方法可以除去混在NaCl固体中的NH4Cl,说明NH4Cl易分解,氯化氢和氨气易发生反应,不是升华,故B错误;
C.二氧化硫一般表现为还原性,与有色物质发生化合反应而漂白,但不稳定,加热时可恢复到原来的颜色,不是氧化还原反应,故C错误;
D.浓硫酸不和H2、Cl2、SO2等气体反应,浓硫酸可用来干燥H2、Cl2、SO2等气体,说明浓硫酸的吸水性,故D正确;
故选D.
点评 本题综合考查元素化合物知识,为高频考点,侧重于基础知识的综合理解和运用的考查,注意相关基础知识的积累,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
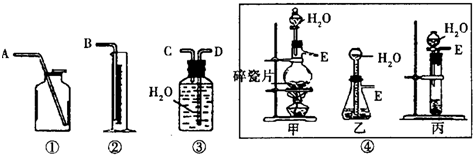
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸遇明火发热爆炸 | |
| B. | 浓硫酸遇水发热爆炸 | |
| C. | 铁与水反应产生氢气,氢气接触空气后遇明火爆炸 | |
| D. | 稀释后的硫酸与铁反应产生氢气接触明火爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 相关信息 |
| X | X的一种单质是自然界硬度最大的晶体 |
| Y | Y的基态原子最外层电子排布式为nsnnpn+1 |
| Z | Z的基态原子L层电子数是K层电子数的3倍 |
| W | W的一种核素的质量数为58,中子数为32 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
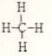 ;X、Z、N形成的原子个数比1:1:1的分子的电子式
;X、Z、N形成的原子个数比1:1:1的分子的电子式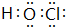 .
.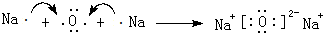 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
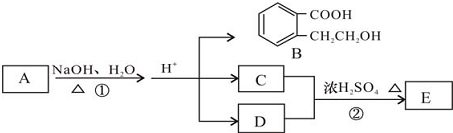
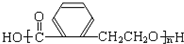 .
.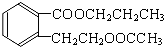 +2 NaOH$\stackrel{△}{→}$
+2 NaOH$\stackrel{△}{→}$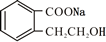 +CH3COONa+CH3CH2CH2OH.
+CH3COONa+CH3CH2CH2OH.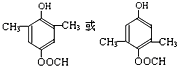 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
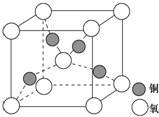 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com